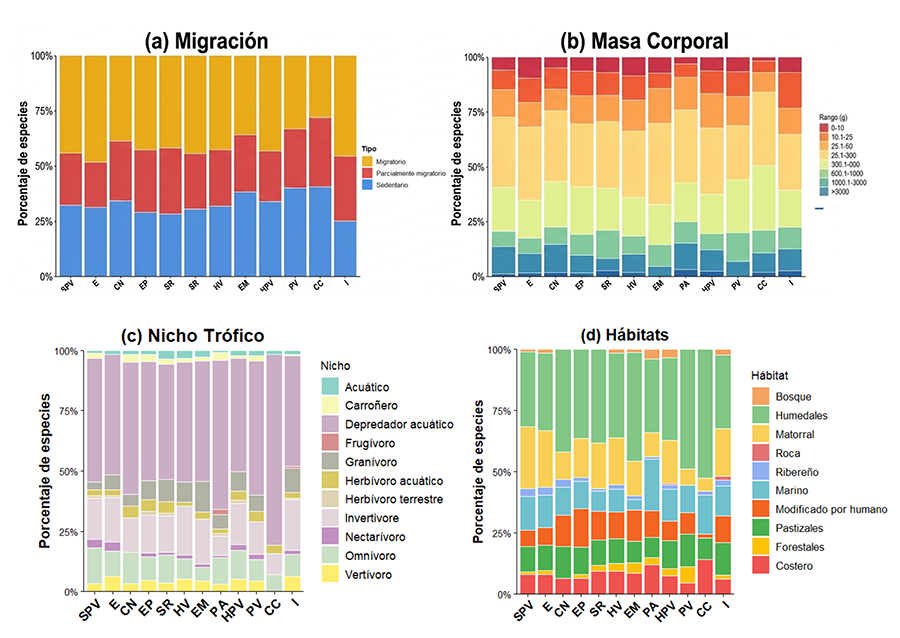
Figura 6. Características funcionales de la
avifauna de los humedales costeros del Perú estudiados (migración, masa
corporal (g), nicho trófico y hábitat). Siglas de los humedales: igual que en
la Figura 2.
Figure 6. Functional
characteristics of the avifauna of the studied coastal wetlands of Peru
(migration, body mass (g), trophic niche, and habitat). Wetland
abbreviations as in Figure
2.
Discusión
Los humedales costeros peruanos sostienen una notable
riqueza aviar (236 especies), confirmando su papel como reservorios críticos de
biodiversidad en el corredor del Pacífico Sur (Barrio
y Guillén, 2014; Plenge, 2024). La composición de
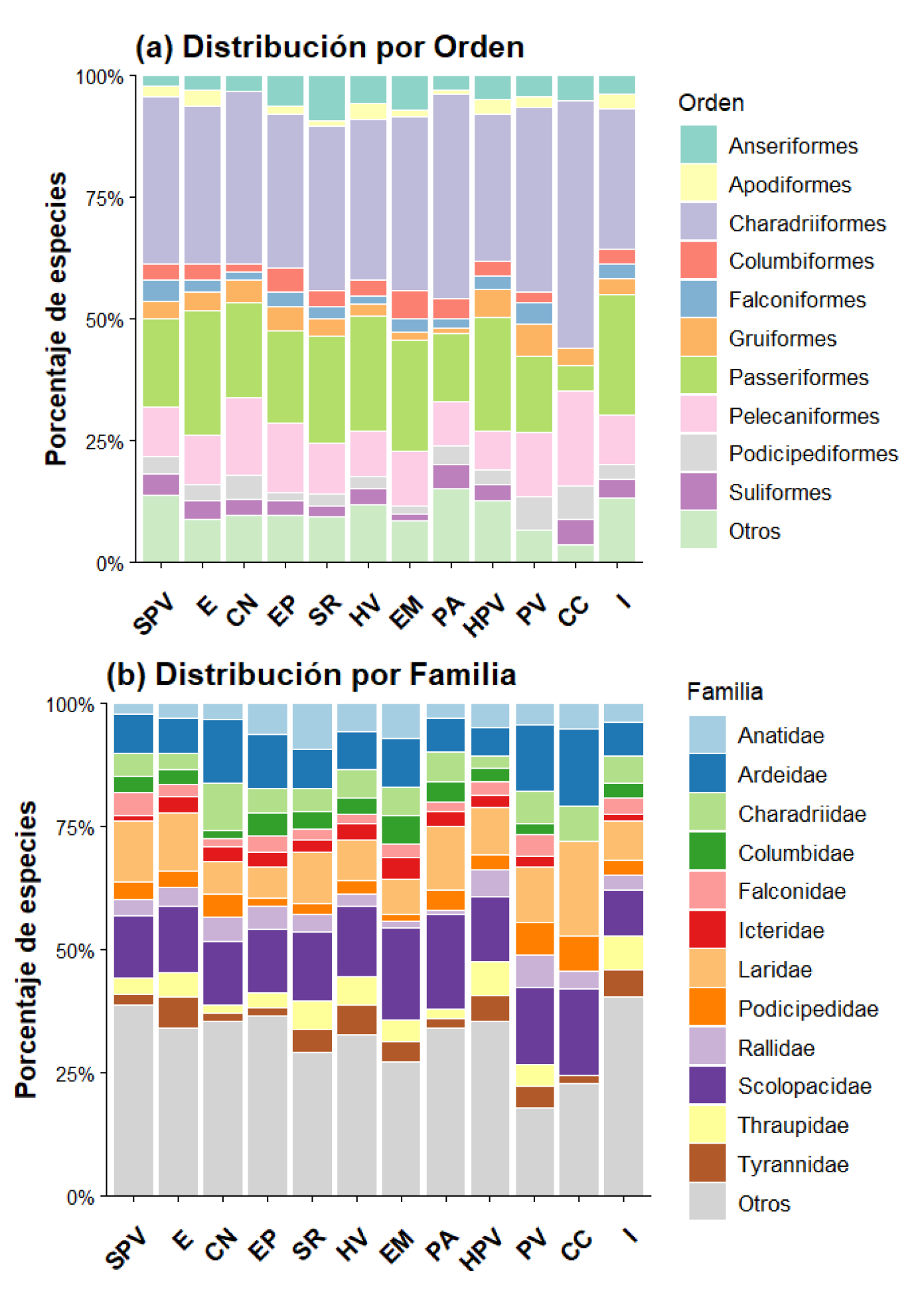
estas comunidades, dominada por Charadriiformes y Passeriformes, refleja un
patrón ecológico recurrente en humedales neotropicales, donde estos grupos
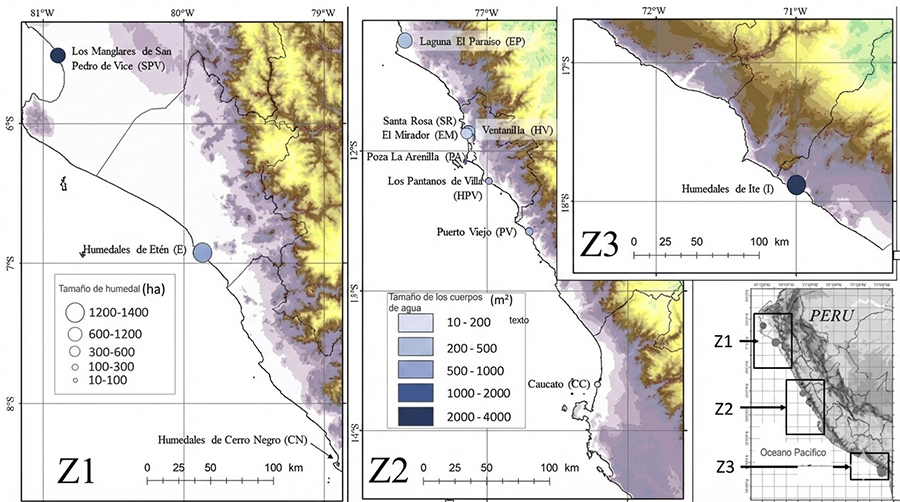
exhiben una marcada especialización en hábitats de interfaz agua-tierra (Schulenberg et al., 2010). Las marcadas diferencias
en riqueza específica entre localidades, como el contraste entre Pantanos de
Villa (211 especies) y Caucato (58 especies), indican que la heterogeneidad y
calidad del hábitat ejercen una influencia determinante más fuerte que la mera
extensión del humedal en la configuración de estas comunidades (Boros et al., 2022). Este equilibrio ecológico, sin
embargo, es susceptible a la presión antrópica, pues la expansión urbana
circundante tiende a fragmentar el paisaje y reducir la disponibilidad de
recursos, homogeneizando los ensamblajes aviares (Chen et
al., 2024).
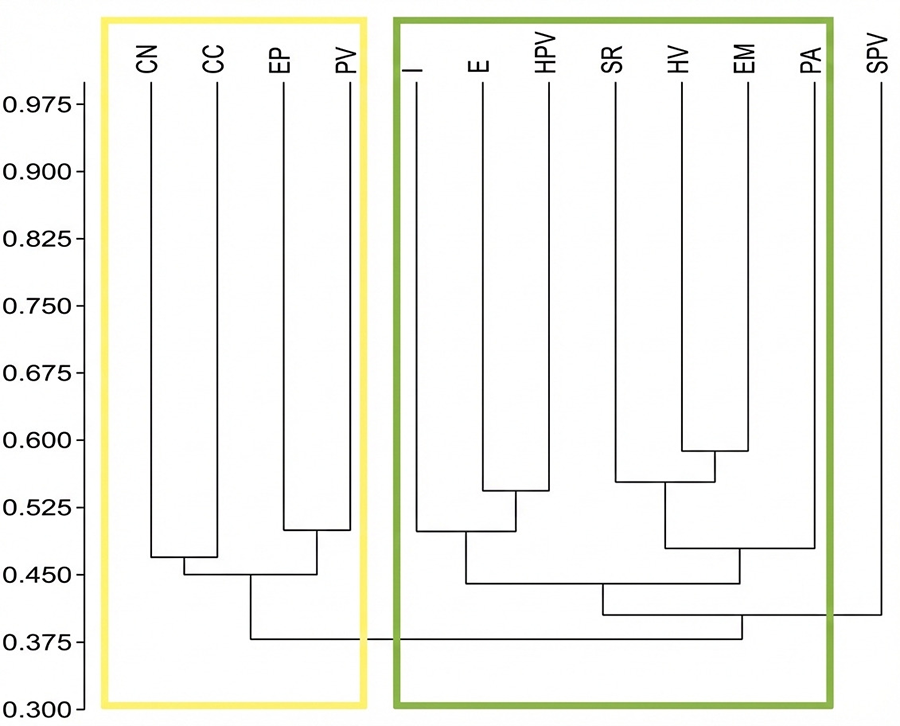
La similitud en la composición de aves entre humedales
distantes geográficamente sugiere que estos ecosistemas funcionan como una red
de parches de hábitat interconectados, facilitando el flujo y el intercambio de
especies a lo largo del litoral (Mitsch y
Gosselink, 2000). Esta conectividad es sostenida, en parte, por especies
generalistas con alta capacidad de dispersión que responden a condiciones
ambientales similares en distintos puntos de la costa (Paillisson
et al., 2002). No obstante, el manglar de San Pedro de Vice representa una
excepción notable, donde la estructura única de la vegetación actúa como un
filtro ambiental que restringe el acceso a la avifauna típica de humedales
abiertos, favoreciendo un ensamble especializado y distintivo (Angulo-Pratolongo et al., 2010). Este hábitat
ofrece recursos de refugio y alimentación particulares, reforzando la premisa
de que la estructura y complejidad de la vegetación son determinantes clave en
la composición de las comunidades (Villavicencio,
2010; Remeš et al., 2021).
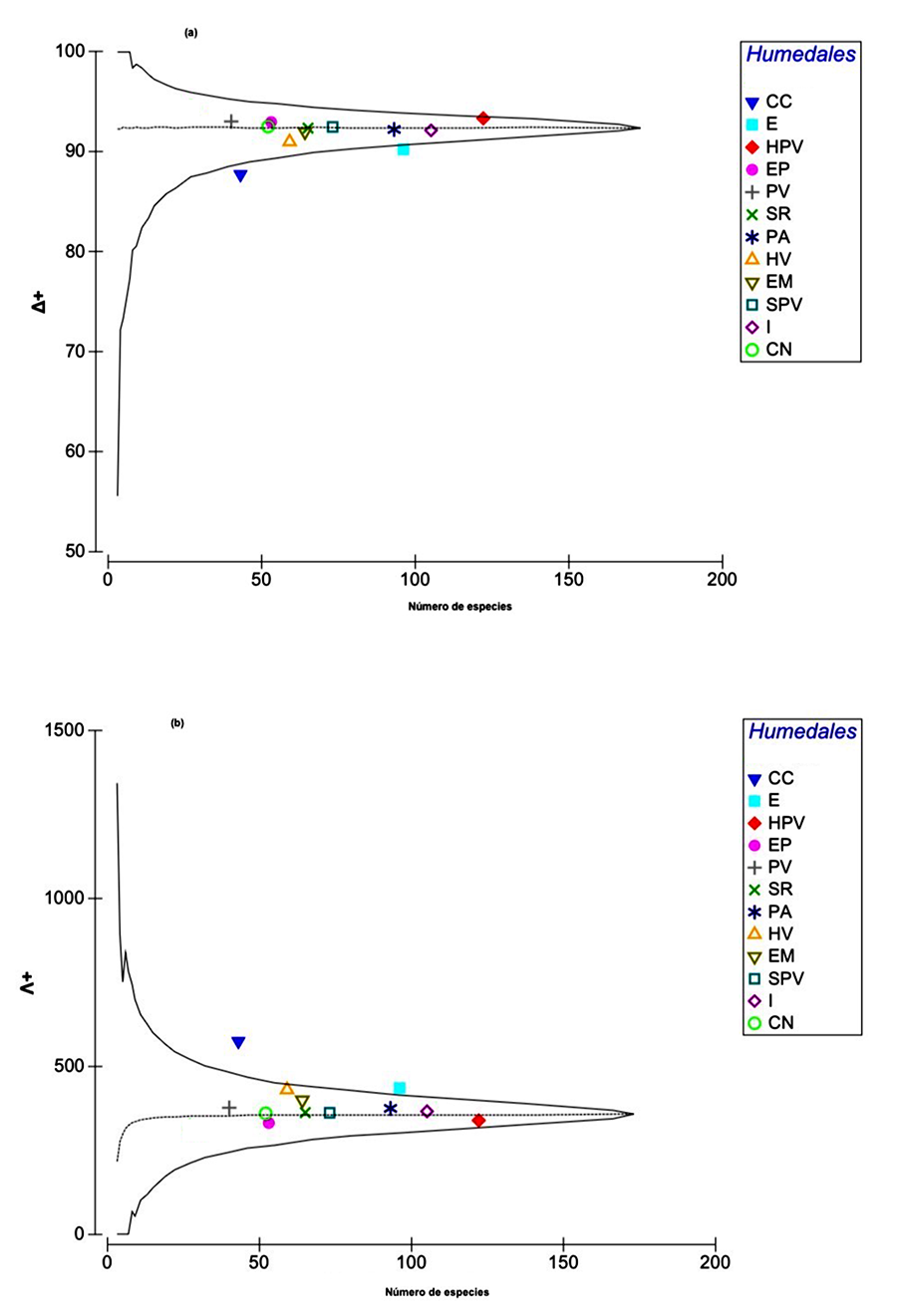
Un hallazgo central de este estudio es la ausencia de
correlación entre la riqueza de especies y la distancia taxonómica promedio (Δ⁺), lo cual demuestra que una
mayor abundancia numérica de especies no se traduce necesariamente en una mayor
diversidad evolutiva, una distinción conceptual fundamental que valida el uso
del índice Δ⁺ (Clarke y Warwick, 2001; Gallão y Bichuette, 2015). Este principio
encuentra respaldo en investigaciones realizadas en otros sistemas de
humedales, donde se ha observado que el conteo de especies es insuficiente para
capturar la complejidad estructural de las comunidades (Li et
al., 2025). En línea con esto, los valores excepcionalmente bajos de Δ⁺ registrados en Caucato
sugieren un proceso de empobrecimiento biótico, comúnmente asociado a sitios
sometidos a una intensa presión antrópica (Requena y
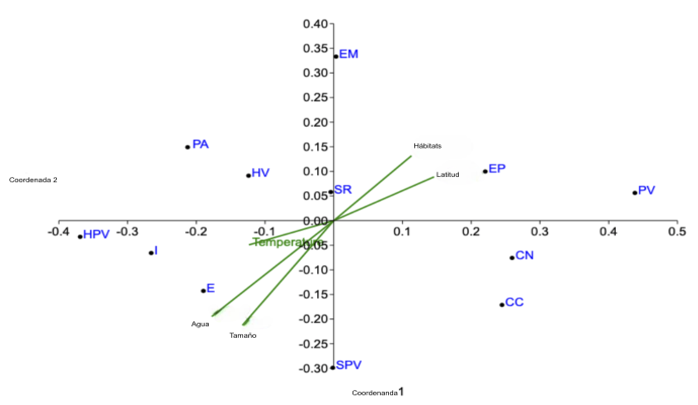
Ramos, 2021). La falta de segregación espacial significativa detectada por
el análisis PERMANOVA refuerza aún más la idea de que los factores locales de
hábitat, más que los gradientes climáticos a macroescala, son los principales
modeladores de estas comunidades (Anderson, 2001; Pohorylow et al., 2016).
Desde una perspectiva funcional, la elevada proporción de
especies migratorias subraya la función de estos humedales como eslabones
críticos dentro de las rutas migratorias del Pacífico, conectándolos con
sistemas ecológicos a escala continental (Aghababyan,
2024). La coexistencia de diversos gremios tróficos sugiere una partición
eficiente de los recursos disponibles (Henry y
Cumming, 2017), aunque esta diversidad funcional es vulnerable a procesos
de homogeneización impulsados por cambios antropogénicos en el uso del suelo (Weeks et al., 2025). La estabilidad de las comunidades
depende directamente de la oferta local de alimento y refugio, haciéndolas
particularmente sensibles a perturbaciones que alteren estos recursos (Becker et al., 2023).
En síntesis, la integración de enfoques taxonómicos (como Δ⁺) y funcionales proporciona
una visión integral que trasciende las limitaciones de los listados de
especies, fundamentando así estrategias de gestión adaptativa más robustas (Smith y Mather, 2012). Resulta prioritario
identificar y proteger sitios con alta distintividad taxonómica para
salvaguardar el valioso capital evolutivo que albergan, un principio central de
la biología de la conservación moderna (Hu et al., 2025).
Esta necesidad es urgente, dada la exposición de los humedales costeros
peruanos a amenazas crecientes, como los incendios recurrentes y la
insuficiencia de los marcos legales de protección (Aponte
et al., 2016; Toledo et al., 2023). La
conservación efectiva de estos ecosistemas requerirá, por tanto, de acciones
integradas que mantengan la conectividad del paisaje, preserven la
heterogeneidad del hábitat y utilicen a las comunidades aviares como
bioindicadores sensibles de su salud ecológica.
Este trabajo, al basarse en una síntesis de datos
secundarios y metadatos, está sujeto a las limitaciones propias de la
heterogeneidad en el esfuerzo y los métodos de muestreo de las fuentes
originales. La ausencia de mediciones ambientales in situ y de datos de otros
componentes del ecosistema restringe la capacidad de inferir relaciones
causales más directas. No obstante, estos resultados establecen una línea base
fundamental para guiar futuros monitoreos estandarizados que validen y
profundicen los patrones aquí descritos.
Conclusiones
Los resultados de este estudio evidencian que la riqueza de
especies y la diversidad taxonómica no siempre varían de manera paralela, lo
que sugiere que los procesos ecológicos y evolutivos que estructuran las
comunidades de aves difieren según las condiciones ambientales y geográficas.
Este hallazgo subraya la necesidad de adoptar enfoques de conservación
multiescalares, que integren indicadores de riqueza, diversidad taxonómica y
rasgos funcionales para evaluar la integridad de los humedales.
La incorporación del análisis funcional aporta una
comprensión más profunda sobre cómo las aves responden a la disponibilidad de
recursos y a las presiones ambientales, destacando la relevancia de proteger
especies clave y mantener la conectividad entre humedales. En este sentido,
identificar y conservar localidades representativas y sitios críticos para la
migración y reproducción resulta esencial para preservar la diversidad
evolutiva y funcional de las aves.
Los humedales evaluados constituyen ecosistemas altamente
dinámicos que sostienen una notable diversidad de aves, moldeada por factores
como el tamaño del humedal, la heterogeneidad de hábitats y la disponibilidad
de recursos tróficos. Estos sistemas desempeñan funciones ecológicas esenciales
como la provisión de alimento, refugio y zonas de descanso que mantienen la
estabilidad y el flujo energético en las redes ecológicas costeras. Por ello,
las estrategias de conservación deben centrarse no solo en proteger la
extensión de los humedales, sino también en preservar la diversidad estructural
y funcional de sus hábitats, asegurando la sostenibilidad a largo plazo de las
comunidades aviares que dependen de ellos. En conjunto, la conservación
efectiva de los humedales costeros peruanos requiere una gestión integrada que
combine protección del hábitat, restauración ecológica y monitoreo continuo de
las comunidades aviares como indicadores del estado ambiental.
Contribución de los autores
FC: concepción del estudio, procesamiento de los
datos y redacción del manuscrito; HA: redacción del manuscrito; CA:
concepción del estudio, procesamiento de datos y redacción del manuscrito.
Disponibilidad de datos y código
Este estudio se basa en la compilación y síntesis de datos
de presencia de aves provenientes de literatura científica publicada y revisada
por pares (ver Referencias). Los datos derivados generados durante esta
investigación, incluyendo la matriz estandarizada de presencia/ausencia, los
índices de diversidad taxonómica (Δ⁺,
Λ⁺) por humedal y los
análisis de variables ambientales, se presentan en las Tablas y Figuras de este
manuscrito y en el Material
Suplementario. La base de datos completa utilizada para los análisis está
disponible Material
Suplementario.
Financiación, permisos requeridos, potenciales
conflictos de interés y agradecimientos
Los autores declaran no tener ningún conflicto de intereses.
Agradecemos el apoyo de María del Pilar Cholan
durante el procesamiento de datos.
Declaración de uso de IA
Se utilizó inteligencia artificial únicamente como
herramienta de apoyo para la revisión de redacción y ortografía, sin influir en
la interpretación de los resultados ni en el contenido científico del
manuscrito.
Referencias
Aghababyan, K. (2024). Birds as potential bioindicators for terrestrial
ecosystems. International Journal of Life Science Research Archive, 6,
1-22. https://doi.org/10.53771/IJLSRA.2024.6.1.0112
Anderson, M. J. (2001). A new method for non-parametric multivariate
analysis of variance. Austral Ecology, 26, 32-46. https://doi.org/10.1111/J.1442-9993.2001.01070.PP.X
Angulo-Pratolongo, F., Schulenberg, T. S., & Puse-Fernández, E. E. (2010). Las
aves de los humedales de Eten, Lambayeque, Perú. Ecología Aplicada, 9(2),
71-81. http://www.scielo.org.pe/scielo.php?script=sci_arttext&pid=S1726-22162010000200002
Aponte, H., Ramírez, W., Lértora, G., Vargas, R., Fernando, G., Carazas,
N., & Liviac, R. (2016). Incendios en los humedales de la costa central del
Perú: Una amenaza frecuente. Científica, 12, 70-81. https://doi.org/10.21142/cient.v12i1.166
Apeño, A. &
Aponte, H. (2022). Caracterización de la diversidad
de aves en un humedal altamente intervenido del Pacífico suramericano. Revista
de la Academia Colombiana de Ciencias Exactas, Físicas y Naturales,
46(179), 380-392. https://doi.org/10.18257/raccefyn.1605
Barrio, J., & Guillén,
C. (2014). Aves de los humedales de la costa peruana. Editorial
Corbidi, Lima, Perú.
Becker, F. K., Boyes, R. S., Wittmer, H., Inman, V., & Marsland, S.
(2023). Landscape-wide pulse events predict trait-based responses among wetland
birds in perennial channels of a dryland wetland. Ecological
Applications, 34, e2931. https://doi.org/10.1002/eap.2931
Boros, E., Inelova, Z., Lánczos, Z., & Végvári, Z. (2022). Waterbird
guilds predict environmental attributes of inland saline aquatic ecosystems on
multi-spatial scales. Science of the Total Environment, 855, 158845. https://doi.org/10.1016/j.scitotenv.2022.158845
Chen, W., Wang, X., Cai, Y., Huang, X., Li, P., Liu, W., ... Hu, C. (2024).
Potential distribution patterns and species richness of avifauna in rapidly
urbanizing East China. Ecology and Evolution, 14, e11515. https://doi.org/10.1002/ece3.11515
Clarke, K. R.,
& Gorley, R. N. (2006). PRIMER v6: User Manual/Tutorial (Plymouth Routines in Multivariate
Ecological Research). PRIMER-E, Plymouth.
Clarke, K.
R., & Warwick, R. M. (1998). A taxonomic
distinctness index and its statistical properties. Journal of Applied
Ecology, 35, 523-531. https://doi.org/10.1046/j.1365-2664.1998.3540523.x
Clarke, K. R.,
& Warwick, R. M. (2001). A further biodiversity
index applicable to species lists: variation in taxonomic distinctness. Marine Ecology Progress Series, 216,
265-278. https://doi.org/10.3354/meps216265
Cruz, Z., Angulo, F., Burger, H. & Borges, R. (2007). Evaluación
de aves en la laguna El Paraíso, Lima, Perú. Revista Peruana de Biología,
14(1), 139-144. https://doi.org/10.15381/rpb.v14i1.2179
Dawyndt, P., De Meyer, H., &
De Baets, B. (2005). UPGMA clustering revisited: A
weight-driven approach to transitive approximation. Journal of Approximate Reasining, 42(3), 174-191. https://doi.org/10.1016/j.ijar.2005.11.001
Gallão, J.
E., & Bichuette, M. E. (2015). Taxonomic distinctness and conservation of a new high biodiversity subterranean area in Brazil. Anais da Academia Brasileira de Ciencias, 87(1), 209-222. https://doi.org/10.1590/0001-3765201520140312
García‐Navas, V., Sattler, T., Schmid, H., & Özgül,
A. (2020). Temporal homogenization of functional and
beta diversity in bird communities of the Swiss Alps. Diversity
and Distributions, 26, 900-911. https://doi.org/10.1111/ddi.13076
Gerónimo-Torres, J. C.,
Barragán-Vázquez, M. R., & Ríos-Rodas, L. (2022). Incorporando la
distintividad taxonómica en estudios de diversidad: Anfibios del Parque Estatal
de la Sierra de Tabasco, México. Ecosistemas, 31, 2294. https://doi.org/10.7818/ECOS.2294
Hammer, Ø., Harper, D. A. T., &
Ryan, P. D. (2001). PAST: Paleontological statistics software
package for education and data analysis. Palaeontologia Electronica, 4,
1-9.
Henry, D. A.,
& Cumming, G. S. (2017). Can waterbirds with
different movement, dietary and foraging functional traits occupy similar
ecological niches? Landscape Ecology, 32, 265-278. https://doi.org/10.1007/s10980-016-0449-8
Hu, Y., Zhou, W., Hu, Y., & Wei, F. (2025). Conservation
evolutionary biology: a unified framework connecting the past, present and
future of biodiversity conservation. Molecular Biology and Evolution,
42, msaf122. https://doi.org/10.1093/molbev/msaf122
Kačergytė, I., Arlt, D., Berg, Å., Żmihorski, M., Knape, J., Rosin, Z. M.,
& Pärt, T. (2021). Evaluating created wetlands for bird diversity and
reproductive success. Biological Conservation, 257, 109084. https://doi.org/10.1016/j.biocon.2021.109084
Li, Y., Xu, H., Wang, X., Yong, X., Li, D., Wu, Y., & Hu,
W. (2025). Multidimensional diversity of birds in different habitats
of the wetland complex in Huaibei Plain, eastern China. Biodiversity
Data Journal, 13, e154264. https://doi.org/10.3897/BDJ.13.e154264
Levene, H. (1960). Robust tests for equality of variances. In: Olkin, I.
(ed) Contributions to probability and statistics, 278-292. Stanford
University Press, Palo Alto.
Mitsch, W.
J., & Gosselink, J. G. (2000). The value of
wetlands: importance of scale and landscape setting. Ecological Economics,
35, 25-33. https://doi.org/10.1016/S0921-8009(00)00165-8
Paillisson, J., Reeber, S., & Marion, L. (2002). Bird
assemblages as bio-indicators of water regime management and hunting
disturbance in natural wet grasslands. Biological Conservation,
106, 115-127. https://doi.org/10.1016/S0006-3207(01)00239-7
Plenge, M. A. (2024). Lista de las
aves del Perú. Unión de Ornitólogos del Perú (UNOP).
Podestá, J., Gil, F.,
Liviac-Espinoza, R., Barona, D., Balarezo-Díaz, A. & Zarate, R. (2021).
Aves de los humedales de la región Callao: actualización y estados de
conservación. The Biologist (Lima), 19(2), 155-173. https://doi.org/10.24039/rtb20211921048
Pohorylow, M. L., Gatto, A., & Lancelotti, J. L. (2016). Caracterización Ambiental y estacional del ensamblaje de aves acuáticas de la meseta del lago Strobel, Patagonia, Argentina. Ornitologia Neotropical, 27, 77-87. https://doi.org/10.58843/ornneo.v27i0.153
Pollack Velásquez, L.E.,
Alvítez Izquierdo, E., Huamán Rodríguez, E.A., Rodríguez Rodríguez, E.F.,
Rimarachín Cayatopa, V. & Vásquez Cabrera, R.C. (2017). Ensamble de aves
del humedal de Cerro Negro, Puerto Morín, La Libertad. Arnaldoa, 24(2),
645-656. https://doi.org/10.22497/arnaldoa.242.24215
Pulido, V. (2018). Ciento quince años
de registros de aves en Pantanos de Villa. Revista Peruana de Biología,
25(3), 291-306. https://doi.org/10.15381/rpb.v25i3.15212
Pulido, V., Salinas, L., del Pino,
J., & Arana, C. (2020). Preferencia de hábitats y estacionalidad de las
especies de aves de los Pantanos de Villa en Lima, Perú. Revista
Peruana de Biología, 27, 349-360. https://doi.org/10.15381/rpb.v27i3.186812
![]() , César Arana2
, César Arana2 ![]() , Héctor Aponte1
, Héctor Aponte1 ![]()