ecosistemas
ISSN 1697-2473
Open access / CC BY-NC 4.0
© 2026 Los autores [ECOSISTEMAS no se hace responsable del uso indebido de material sujeto a derecho de autor] / © 2026 The authors [ECOSISTEMAS is not responsible for the misuse of copyrighted material]
Ecosistemas 35(1): 3114 [enero - abril / January - April, 2026]: https://doi.org/10.7818/ECOS.3114
Editor asociado / Associate editor: Jorge Garrido-Bautista
ARTÍCULO DE REVISIÓN / REVIEW ARTICLE
Ecofisiología de reptiles en un mundo cambiante: integrando las respuestas funcionales al cambio climático y de uso de suelo
Francisco J. Muñoz-Nolasco1,2,3,* ![]() , Víctor L. Barradas2
, Víctor L. Barradas2 ![]() , Andrés García4
, Andrés García4 ![]() , Fausto R. Méndez-de la Cruz5
, Fausto R. Méndez-de la Cruz5 ![]()
(1) Posgrado en Ciencias Biológicas, Universidad Nacional Autónoma de México, Unidad de Posgrado, Edificio D, 1° Piso, Circuito de Posgrados, Ciudad Universitaria, Coyoacán, C. P. 04510, Ciudad de México, México.
(2) Laboratorio de Interacción Planta-Atmósfera, Departamento de Ecología Funcional, Instituto de Ecología, Universidad Nacional Autónoma de México, Ciudad Universitaria, C. P. 04510, Ciudad de México, México.
(3) Unión de Especialistas en Biodiversidad, Conservación y Sustentabilidad (Unesbio), A. C., C. P. 45178, Zapopan, Jalisco, México.
(4) Estación de Biología Chamela, Instituto de Biología, Universidad Nacional Autónoma de México, C. P. 48980, San Patricio, Jalisco, México.
(5) Laboratorio de Herpetología, Departamento de Zoología, Instituto de Biología, Universidad Nacional Autónoma de México, C.P. 04510, Coyoacán, Ciudad de México, México.
* Autor de correspondencia / Corresponding author: F. J. Muñoz-Nolasco [fjmn36@gmail.com]
|
> Recibido / Received: 12/09/2025 – Aceptado / Accepted: 12/02/2026 |
Cómo citar / How to cite: Muñoz-Nolasco, F. J., Barradas, V. L., García, A., & Méndez-de la Cruz, F. R. (2026). Ecofisiología de reptiles en un mundo cambiante: integrando las respuestas funcionales al cambio climático y de uso de suelo. Ecosistemas 35(1): 3114. https://doi.org/10.7818/ECOS.3114
|
Ecofisiología de reptiles en un mundo cambiante: integrando las respuestas funcionales al cambio climático y de uso de suelo Resumen: El cambio climático y el cambio de uso de suelo constituyen dos de las principales amenazas a la biodiversidad. Como ectotermos, los reptiles son unos de los grupos más sensibles a las alteraciones en las condiciones térmicas e hídricas de su entorno. Por lo tanto, la ecofisiología se ha posicionado como una disciplina crucial para comprender las posibles respuestas funcionales de estos organismos a las alteraciones ambientales. Aunque históricamente las investigaciones sobre ecofisiología de reptiles se han centrado en aspectos térmicos, cada vez más se reconoce la importancia de la hidrorregulación para este grupo de vertebrados. A través de una síntesis crítica (narrativa) de la literatura reciente, evaluamos cómo las alteraciones antrópicas en el ambiente físico impactan la fisiología de los reptiles, con consecuencias que abarcan desde su comportamiento, reproducción, distribución, interacciones bióticas y riesgo de extinción. Nos centramos en el cambio climático y de uso de suelo por ser los principales determinantes de la alteración de las condiciones biofísicas del hábitat y por su impacto en la fisiología térmica e hídrica de los reptiles. Discutimos la utilidad de adoptar aproximaciones basadas en modelos biofísicos y rasgos funcionales para ofrecer una perspectiva más profunda de los mecanismos subyacentes a las respuestas de los organismos. Finalmente, proponemos líneas de investigación que hasta ahora no han sido exploradas lo suficientemente, pero que plantean la posibilidad de contribuir sustancialmente a la conservación de este grupo de organismos. Palabras clave: cambio global; ectotermos; fisiología; hidroregulación; termoregulación Ecophysiology of reptiles in a changing world: integrating functional responses to climate and land use change Abstract: Climate change and land-use change constitute two of the main threats to biodiversity. As ectotherms, reptiles are among the most sensitive groups to alterations in the thermal and hydric conditions of their environment. Therefore, ecophysiology has positioned itself as a crucial discipline for understanding the potential functional responses of these organisms to environmental disturbances. Although research on reptile ecophysiology has historically focused on thermal aspects, the importance of hydroregulation for this vertebrate group is increasingly recognized. Through a critical (narrative) synthesis of recent literature, we evaluate how anthropogenic alterations in the physical environment impact reptile physiology, with consequences ranging from behaviour, reproduction, and distribution to biotic interactions and extinction risk. We focus on climate change and land-use change as they are the primary drivers of alterations in habitat biophysical conditions and their impact on thermal and hydric physiology of reptiles. We discuss the utility of adopting approaches based on biophysical models and functional traits to offer a deeper perspective on the mechanisms underlying organismal responses. Finally, we propose research lines that have not yet been sufficiently explored but hold the potential to contribute substantially to the conservation of this group of organisms. Keywords: global change; ectotherms; physiology; hydroregulation; thermoregulation |
Los cambios ambientales y la fisiología de los organismos
Las alteraciones ambientales antrópicas, tales como el cambio de uso de suelo y el cambio climático, modifican los componentes abióticos (e.g. temperatura, humedad, radiación solar) y bióticos (e.g. cobertura vegetal, abundancias relativas, interacciones intra- e interespecíficas) de los ecosistemas (Somero, 2012; Blois et al., 2013). Esta modificación en las condiciones ambientales puede inducir estrés fisiológico y repercutir sobre el comportamiento y el estado de salud de los organismos, lo cual puede, a su vez, afectar las tasas de mortalidad y resultar en el eventual colapso de las poblaciones (Tracy et al., 2006; Sinervo et al., 2010). Por lo tanto, indagar en las capacidades y límites fisiológicos de los organismos es crucial para comprender sus posibles respuestas a los estresores ambientales antrópicos y anticipar efectos en los ensamblajes y en el funcionamiento de los ecosistemas (Nowakowski et al., 2018a). En consecuencia, indagar en las capacidades fisiológicas es vital para fortalecer las medidas de conservación ya existentes, tales como el diseño de corredores biológicos climáticamente resilientes o la selección de sitios para translocaciones (Tracy et al., 2006; Cooke et al., 2014; Fitzgerald et al., 2018).
Por supuesto, no todos los organismos poseen las mismas capacidades de ajuste a las alteraciones ambientales. En el caso de los animales, numerosos estudios han señalado que los ectotermos son particularmente vulnerables al cambio climático y al cambio de uso de suelo, debido a que sus funciones biológicas básicas dependen estrechamente de la temperatura ambiental, la cual se ve modificada como consecuencia de dichos fenómenos (Deutsch et al., 2008; Huey et al., 2009; Nowakowski et al., 2018a; Quintero-Pérez et al., 2023). Entre los ectotermos, los reptiles no avianos (“reptiles”, de aquí en adelante) han destacado como modelos de estudio para poner a prueba numerosas hipótesis ecofisiológicas y para evaluar cómo los cambios ambientales impactan a la biodiversidad (Winter et al., 2016; Taylor et al., 2021). Su diversidad evolutiva y ecológica, su sensibilidad a la perturbación ambiental y la facilidad con la que pueden ser manejados y estudiados en campo y en laboratorio hacen de ellos modelos idóneos en investigación (Taylor et al., 2021; Schwarzkopf, 2022). Es por ello por lo que múltiples estudios han sido dirigidos a evaluar la vulnerabilidad de este grupo de vertebrados a diferentes disturbios ambientales y su riesgo de extinción (Sinervo et al., 2010; Böhm et al., 2016; Senior et al., 2021; Farooq et al., 2024). Cabe destacar que, aunque el marco conceptual aquí discutido es aplicable a los reptiles en su conjunto, la mayoría de la evidencia empírica disponible proviene de taxones del orden Squamata (lagartijas y serpientes; “escamosos”). Por lo tanto, gran parte de los estudios de caso y ejemplos abordados en esta revisión se centran en este grupo, el cual ha sido el foco predominante en la literatura ecofisiológica actual.
Determinar la vulnerabilidad de los organismos a las modificaciones ambientales es una tarea compleja que requiere la integración de diversos factores, tanto intrínsecos como extrínsecos (Murray et al., 2014; Chichorro et al., 2022). En este sentido, Williams y colaboradores (2008) propusieron que la vulnerabilidad de una especie a los cambios ambientales depende de: 1) su sensibilidad a dichos cambios, 2) su exposición a ellos, 3) su resiliencia o habilidad para recuperarse de las perturbaciones y 4) su potencial de adaptación al cambio. Lamentablemente, esta propuesta requiere información exhaustiva, y rara vez disponible, de la fisiología, el comportamiento y la genética de los organismos. Como alternativa, Huey y colaboradores (2012) propusieron el uso de atributos ecofisiológicos de fácil cuantificación (como las preferencias y tolerancias térmicas) para evaluar la vulnerabilidad ante el cambio climático y de uso de suelo, dado que ambos fenómenos alteran directamente la biología térmica de los organismos. Algunos autores incluso han sugerido la estimación de curvas de desempeño térmico para tal fin, que, aunque son más laboriosas de obtener, pueden ofrecer información aún más precisa (Tüzün y Stoks, 2018). El integrar atributos fisiológicos térmicos ha mostrado ser útil para determinar el riesgo de extinción en reptiles, pues estos parámetros suelen proveer una explicación causal directa entre la biología de estos organismos, los impactos a su hábitat y el estado de sus poblaciones (Sinervo et al., 2010; Pontes-da-Silva et al., 2018; Muñoz-Nolasco et al., 2023).
Por el contrario, los aspectos de hidrorregulación han sido relativamente menos estudiados en este grupo de vertebrados (Pirtle et al., 2019; Rozen-Rechels et al., 2019; Le Galliard et al., 2021), esto a pesar de que el cambio climático y el cambio de uso de suelo modifican los regímenes pluviales y la disponibilidad de agua en los ecosistemas terrestres (Dai et al., 2018; Te Wierik et al., 2021). Este sesgo literario podría derivar de la idea tradicional de que el huevo amniota y el tegumento queratinizado confieren a los reptiles una independencia casi total de las restricciones hídricas ambientales. No obstante, dicha noción ha sido cuestionada, lo que sugiere que la sensibilidad hídrica de este grupo es mayor de lo que se asumía originalmente (Roberts y Lillywhite, 1980; Skulan, 2000). Si bien, comparados con los anfibios, los reptiles han evolucionado atributos que los hacen menos dependientes del agua libre (Lillywhite, 2016; Murphy y DeNardo, 2019), muchas especies, sobre todo aquellas de ambientes mésicos (i.e. húmedos y térmicamente estables), suelen poseer capacidades limitadas de conservación de agua (Muñoz-Nolasco et al., 2019; Pirtle et al., 2019), y aun aquellas de ambientes xéricos (i.e. áridos) pueden depender de fuentes de agua bebible para satisfacer sus requerimientos hídricos (Murphy y DeNardo, 2019). De hecho, las tasas de pérdida de agua y el grado de dependencia al agua han sido identificadas como unos de los principales predictores de la vulnerabilidad de los reptiles a las modificaciones de su hábitat (Griffis-Kyle et al., 2018; Nowakowski et al., 2018a; Camacho et al., 2023), lo que destaca la importancia de la fisiología hídrica en el contexto de los disturbios antrópicos.
Por lo general, las alteraciones sobre los ambientes térmico e hídrico no impactan de manera aislada sobre la fisiología, sino que actúan concomitantemente (Camacho et al., 2023). El aumento en la temperatura ya sea debido al cambio climático o a la pérdida de cobertura vegetal, incrementa el déficit de presión de vapor del aire (Grossiord et al., 2020), lo que a su vez aumenta las tasas de pérdida de agua por evaporación (PAE) de los organismos (Weaver et al., 2023). Esto puede conducir a un estado de deshidratación, que además de tener implicaciones directas sobre la fisiología y la supervivencia de los reptiles, suele conllevar compromisos (trade-offs) entre el balance hídrico y la termorregulación (Pirtle et al., 2019; Camacho et al., 2023). En este sentido, se ha observado que los organismos deshidratados llegan a manifestar una disminución en sus preferencias y tolerancias térmicas (Plummer et al., 2003; Sannolo y Carretero, 2019; Camacho et al., 2023), presumiblemente a fin de reducir las tasas de PAE. No obstante, la PAE puede constituir también un mecanismo de emergencia para amortiguar el calentamiento por medio de enfriamiento por evaporación (Loughran y Wolf, 2020). Es de crucial importancia documentar estos rasgos a nivel específico, ya que la magnitud de tales compromisos puede variar incluso entre especies simpátricas y cercanamente emparentadas (Sannolo et al., 2018).
Efectos aditivos y sinérgicos del cambio climático y el cambio de uso de suelo sobre la fisiología de los reptiles
La evidencia de los efectos adversos del cambio climático antrópico sobre la biodiversidad y el funcionamiento de los ecosistemas es contundente (Habibullah et al., 2022; Shivanna, 2022); sin embargo, su impacto no es uniforme a escalas geográfica y taxonómica. Si bien la tasa de calentamiento es más pronunciada a mayores latitudes, se ha señalado que los ectotermos tropicales son los más vulnerables al calentamiento global, debido a que presentan límites de tolerancia térmica más estrechos que los de regiones templadas y a que ocupan hábitats con temperaturas ya cercanas a su óptimo fisiológico (Deutsch et al., 2008; Tewksbury et al., 2008; Huey et al., 2009). De manera similar, los organismos de tierras bajas se encuentran en riesgo de sufrir los efectos de las altas temperaturas debido a que experimentan una menor variación térmica que los de altas elevaciones, por lo cual su capacidad de tolerar temperaturas extremas es menor (Sunday et al., 2019). No obstante, se ha documentado que los ámbitos de distribución altitudinal de muchas especies se están desplazando hacia mayores elevaciones debido al calentamiento (Freeman et al., 2018; Feldmeier et al., 2020; Chen et al., 2025). Ya que este escalamiento hacia cotas altitudinales mayores no puede continuar indefinidamente, se considera que las especies de montaña adaptadas al frío podrían enfrentar un riesgo de extinción aun mayor debido a la disminución de sus hábitats (Freeman et al., 2018); aunque el desplazamiento hacia laderas con orientación septentrional (menos expuestas a la radiación solar y al calentamiento) podría representar otra opción ante el incremento de temperaturas (Feldmeier et al., 2020). Sin embargo, cabe aclarar que las condiciones en altitud no son meramente un reflejo más frío de las tierras bajas. Factores ambientales relevantes como la disminución de la presión parcial de oxígeno (PO2) y el incremento en la intensidad de la radiación ultravioleta (UV) imponen severos desafíos fisiológicos y de desempeño que pueden limitar la capacidad de las especies para establecerse exitosamente en nuevas elevaciones (Gangloff et al., 2019; Serén et al., 2025).
Si bien el aumento de temperaturas puede conducir directamente a una mayor mortalidad debido al sobrecalentamiento (Rubalcaba y Olalla-Tárraga, 2020), la restricción en los horarios de actividad podría ser la principal causa del colapso poblacional asociada al cambio climático (Sinervo et al., 2010) (Fig. 1). De acuerdo con esta hipótesis, el aumento en la temperatura restringe los horarios en los que los organismos pueden emerger de sus refugios para termorregular, forrajear y reproducirse, actividades cruciales para el mantenimiento de las poblaciones (Sinervo et al., 2010). Este mecanismo ha sido usado para explicar extirpaciones recientes y la distribución geográfica de algunas especies de reptiles, así como para evaluar su riesgo de extinción (Sinervo et al., 2010; Pontes-da-Silva et al., 2018; Caetano et al., 2020; Muñoz-Nolasco et al., 2023). No obstante, algunos cuestionamientos en torno a esta hipótesis plantean que ignorar aspectos de cobertura vegetal podría limitar la precisión de las estimaciones (Kearney, 2013).
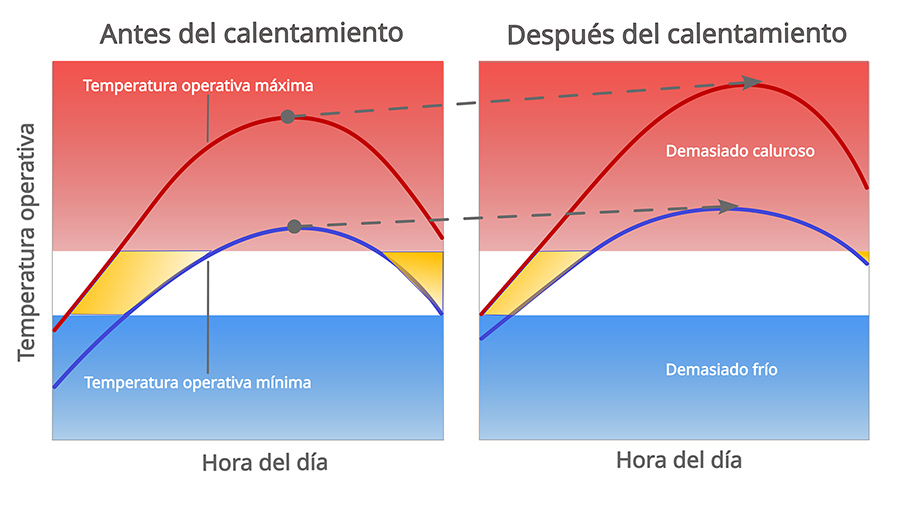
Figura 1. Con calentamiento, el horario de actividad de los ectotermos se reduce, lo que limita el tiempo que los organismos pueden dedicar a obtener la energía necesaria para la reproducción. A la larga, se puede conducir al colapso poblacional y a la extinción. La imagen muestra el aumento en las temperaturas operativas mínimas y máximas (líneas azules y rojas, respectivamente) y la consecuente reducción en los umbrales térmicos de actividad (zonas ámbar) en un escenario de calentamiento. Modificado de Huey et al. (2010).
Figure 1. With warming, the activity period of ectotherms is reduced, limiting the time organisms can dedicate to obtaining the energy necessary for reproduction. Over time, this can lead to population collapse and extinction. The image shows the increase in minimum and maximum operative temperatures (blue and red lines, respectively) and the consequent reduction in thermal activity thresholds (amber zones) in a warming scenario. Modified from Huey et al. (2010).
En comparación con el cambio climático, existen muchas menos investigaciones en torno a los efectos del cambio de uso de suelo sobre la fisiología de los reptiles. Este sesgo es preocupante, pues el cambio de uso de suelo es considerado la principal causa de la pérdida de biodiversidad actual y una de las que más afecta a los reptiles a nivel global (Keinath et al., 2017; Cordier et al., 2021; Jaureguiberry et al., 2022). Las modificaciones antrópicas del hábitat, tales como la pérdida de cobertura vegetal, su reemplazo por vegetación no nativa o la urbanización, generan a menudo condiciones microclimáticas desafiantes para los organismos (Hall y Warner, 2018; García y Clusella-Trullas, 2019; Lara-Reséndiz et al., 2024). A estas alteraciones se suman los incendios forestales, los cuales también modifican el microclima a nivel local, afectan las tasas de supervivencia y simplifican la complejidad de los ensamblajes de reptiles (Ferreira et al., 2016). Por lo general, solamente las especies más tolerantes a las altas temperaturas y a la deshidratación pueden persistir ante dichos cambios (Frishkoff et al., 2015; Ferreira et al., 2016; Nowakowski et al., 2018a; Fig. 2). No obstante, se ha observado que algunas especies son capaces de ajustar sus tasas metabólicas y de pérdida de agua en ambientes urbanizados (Vardi et al., 2023), lo que sugiere que la plasticidad podría, hasta cierto punto, permitir el mantenimiento de las poblaciones de reptiles en hábitats antropizados.
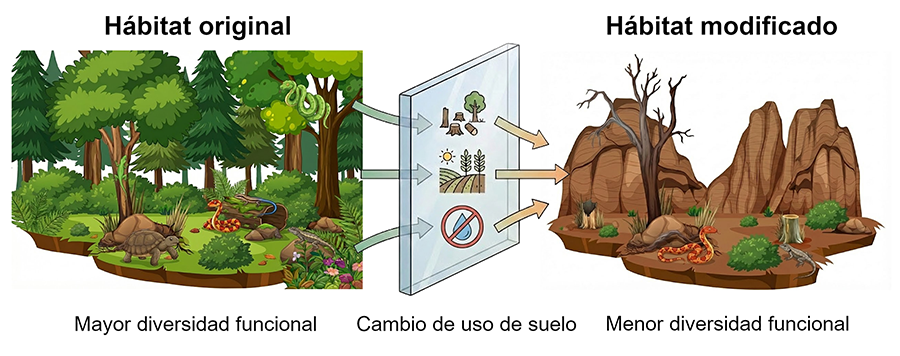
Figura 2. El cambio de uso de suelo actúa como filtro ambiental que modifica las condiciones biofísicas de los hábitats, tales como la radiación solar, la temperatura y la disponibilidad de agua. Este proceso selecciona a las especies más tolerantes al estrés térmico y a la deshidratación, lo que resulta en una pérdida de diversidad funcional.
Figure 2. Land use change acts as an environmental filter that modifies the biophysical conditions of habitats, such as solar radiation, temperature, and water availability. This process selects for species that are most tolerant to thermal stress and dehydration, resulting in a loss of functional diversity.
Pese a que el cambio climático y las modificaciones de hábitat actúan simultáneamente, estos dos factores de cambio global rara vez son estudiados en conjunto (Nowakowski et al., 2018b). La disminución en la disponibilidad de sombra provista por la cobertura vegetal puede exacerbar los impactos del calentamiento global sobre los umbrales de actividad de los reptiles (Kearney, 2013; Lara-Reséndiz et al., 2024). Las especies de distribución restringida y especialistas de hábitat son especialmente proclives debido a su limitado potencial desplazamiento hacia sitios con condiciones microclimáticas más benignas (Keinath et al., 2017; Jiménez-Robles y De la Riva, 2019; Muñoz-Nolasco et al., 2023). Además, pese a que el calentamiento climático se asocia con ascensos altitudinales en la distribución de los organismos, en un estudio preliminar se documentó que algunas lagartijas se están desplazando hacia elevaciones más bajas debido a la mayor presión de deforestación en zonas altas (Battey et al., 2019). Asimismo, el aumento en la temperatura global y en la frecuencia y severidad de las sequías están relacionados con una mayor mortalidad en plantas, lo cual modifica la estructura de los hábitats y potencia los efectos del cambio climático a escalas locales y regionales (Grossiord et al., 2020).
Implicaciones del cambio global sobre la fisiología de la reproducción
Las modificaciones ambientales antrópicas tienen amplias consecuencias sobre la fisiología reproductora de los reptiles (Fig. 3). Por ejemplo, se ha sugerido que los reptiles escamosos de montaña y alta montaña podrían ser más vulnerables al cambio climático debido a la prevalencia del modo reproductor vivíparo a altas elevaciones (Pincheira‐Donoso et al., 2013; Domínguez-Guerrero et al., 2022). Las especies vivíparas están en mayor riesgo debido a que presentan parámetros térmicos más bajos que las ovíparas, lo que las hace más sensibles a las reducciones en sus umbrales térmicos de actividad por altas temperaturas (Sinervo et al., 2010; Wang et al., 2017). Aunado a lo anterior, dado que la viviparidad es menos viable en ambientes cálidos y a que la reversión a la oviparidad es poco probable (Whittington et al., 2022), este modo reproductor podría constituir un callejón sin salida evolutivo ante al calentamiento global (Pincheira‐Donoso et al., 2013). Sin embargo, existen casos documentados de re-evolución de la oviparidad en lagartijas, lo que desafía la noción de la irreversibilidad evolutiva (Recknagel et al., 2018). Esto no quiere decir que las especies vivíparas estén totalmente indefensas a los efectos del cambio climático. Por el contrario, la termorregulación conductual materna es capaz de amortiguar los efectos de las fluctuaciones térmicas durante la gestación, lo que explicaría el éxito de la viviparidad en ambientes térmicamente heterogéneos (Foucart et al., 2018). En el caso de las especies ovíparas, ahora se sabe que los embriones no son pasivos ante las variaciones ambientales, sino que pueden lidiar con los desafíos abióticos por medio de plasticidad fisiológica y conductual (Du y Shine, 2015).
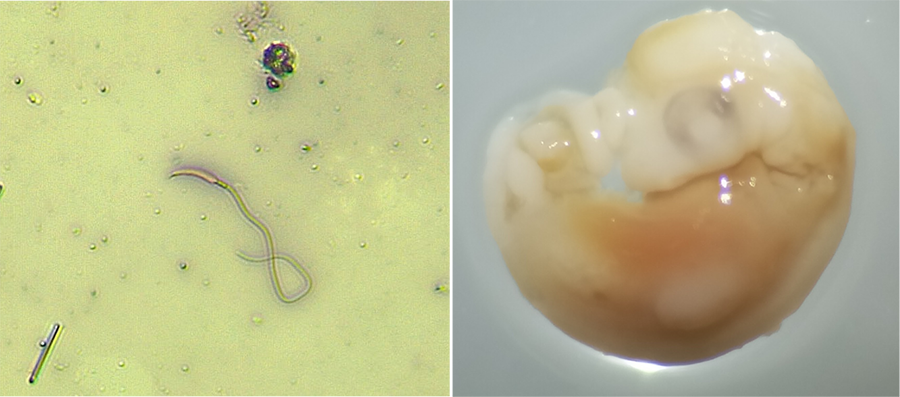
Figura 3. La temperatura influye fuertemente en la maduración espermática y el desarrollo embrionario de los reptiles. Izquierda: espermatozoide de Sceloporus cozumela; derecha: embrión de S. exsul.
Figure 3. Temperature strongly influences sperm maturation and embryonic development in reptiles. Left: spermatozoon of Sceloporus cozumela; right: embryo of S. exsul.
Algunas especies de reptiles, particularmente los crocodilios, testudines, el tuátara y algunos escamosos, presentan determinación sexual por temperatura (DST) (Cornejo-Páramo et al., 2020). Se ha sugerido que este sistema de determinación sexual constituye una desventaja frente al cambio climático (Valenzuela et al., 2019), pues el incremento en las temperaturas de incubación/gestación (o su disminución por la incidencia de fenómenos hidrometeorológicos extremos (Charruau et al., 2010)), conduciría a un sesgo en la descendencia hacia cierto sexo, y eventualmente al colapso poblacional. No obstante, en el caso de las tortugas marinas, se ha propuesto que la DST podría representar en realidad un mecanismo para el mantenimiento de las poblaciones ante extremos térmicos (Santidrián-Tomillo y Spotila, 2020). De acuerdo con esta hipótesis, cuando la supervivencia de las crías disminuye por altas temperaturas, se produce el sexo que incrementa la fecundidad futura (i.e. las hembras), lo que incrementa la resiliencia al cambio climático (Santidrián-Tomillo y Spotila, 2020). Por otra parte, en dos especies de escamosos vivíparos (Zootoca vivipara y Vipera aspis) la restricción hídrica durante el desarrollo embrionario puede anular la determinación sexual cromosómica y producir una mayor proporción de crías con fenotipo masculino (Dupoué et al., 2019). El descubrimiento de este modo de determinación sexual es relativamente reciente y, contrario a la DST, no ha podido ser asociado aún con alguna función adaptativa (Dupoué et al., 2019).
Las modificaciones en el ambiente térmico e hídrico pueden influir sobre el fenotipo de las crías más allá de su sexo; sin embargo, las normas de reacción a estos factores varían considerablemente en función de los rasgos fenotípicos y los taxones (Noble et al., 2018). La exposición durante la incubación/gestación a altas temperaturas tiende a afectar la talla y forma corporal, las reservas energéticas, el desempeño locomotor y el comportamiento de termorregulación de las crías (Singh et al., 2020), con implicaciones usualmente negativas sobre la adecuación (pero ver Amiel y Shine (2012)). Los efectos de la restricción hídrica en este sentido son menos conocidos, pero se sabe que pueden conducir a una mayor mortalidad de los embriones, a un conflicto materno-embrional y a alteraciones en el comportamiento de las crías (Rozen-Rechels et al., 2018; Dupoué et al., 2020; Dezetter et al., 2021). Cabe resaltar que los costos hídricos asociados a la reproducción son menores en especies ovíparas que en vivíparas, por lo que se ha propuesto que la oviparidad puede representar una estrategia para economizar agua en ambientes xéricos (Dupoué et al., 2020). No obstante, la viviparidad también está ampliamente documentada en zonas áridas, donde se considera una estrategia alternativa para proteger los embriones de la deshidratación extrema del suelo al retenerlos en el ambiente acuoso del saco gestacional (Bonnet et al., 2017).
Un aspecto que ha sido aún poco estudiado en reptiles son los límites de fertilidad térmicos (LFT) (Quintero-Pérez et al., 2023). Diversas investigaciones llevadas a cabo en ectotermos sugieren que los LFT son sumamente sensibles a temperaturas subletales, por lo que la mayoría de las evaluaciones de vulnerabilidad podrían subestimar el riesgo de extinción por cambio climático (Parratt et al., 2021; Bretman et al., 2024). La exposición a temperaturas incluso dentro de los intervalos de preferencia o desempeño térmico máximo puede producir anomalías en la morfología espermática, baja concentración de espermas y disminuir la motilidad y viabilidad espermática (Quintero-Pérez et al., 2023). Este desfase en los distintos óptimos térmicos indica la existencia de patrones de coadaptación complejos entre los atributos fisiológicos de los organismos (Angilletta Jr. et al., 2006), patrones que hasta ahora no han sido explorados suficientemente. Más aún, se ha propuesto que los patrones de distribución de algunas especies de ectotermos podrían estar definidos más por los límites térmicos en la reproducción que por los límites de temperatura letales (Parratt et al., 2021).
Finalmente, un aspecto crucial pero históricamente desatendido en torno a las implicaciones del cambio climático sobre la reproducción es la ecología sensorial y las señales sexuales en reptiles (y en animales en general). Los sistemas de comunicación intraespecífica evolucionan para maximizar su eficacia en condiciones climáticas específicas, pero se predice que los cambios ambientales rápidos superarán la capacidad de adaptación evolutiva del diseño de la señal (Endler y Basolo, 1998). En este sentido, un estudio experimental realizado con lagartijas de montaña (Iberolacerta cyreni) mostró que la eficacia (i.e. la detectabilidad y persistencia) de las señales químicas sexuales (secreciones femorales) disminuye significativamente bajo condiciones de alta temperatura (Martín y López, 2013). Los autores encontraron que las áreas marcadas con olor y expuestas a altas temperaturas no eran seleccionadas por las hembras, lo que sugiere que el aumento en las temperaturas ambientales podría limitar la eficacia de la quimiorecepción y, consecuentemente, afectar la selección sexual (Martín y López, 2013). Esta es, en definitiva, un área que amerita mayor investigación.
Ecofisiología y la reestructuración antrópica de los ensamblajes
La mayoría de las estimaciones acerca del impacto de las modificaciones antrópicas sobre la biodiversidad se basan en una o unas cuantas especies, a menudo de distintas localidades (Phillips et al., 2020). No obstante, las consecuencias más ostensibles de los cambios ambientales se dan a nivel de los ensamblajes locales (Chown, 2023). En este sentido, los enfoques basados en rasgos funcionales pueden revelar información importante sobre la estructura de los ensamblajes y revelar patrones emergentes que los estudios interespecíficos suelen pasar por alto (Phillips et al., 2020; Chown, 2023). Una de las ventajas de los enfoques basados en rasgos funcionales sobre aquellos basados en identidades taxonómicas de las especies es que los primeros permiten profundizar e indagar en las dinámicas ecológicas que subyacen los procesos de ensamblaje y el funcionamiento de las comunidades animales (De Bello et al., 2021; Brandl et al., 2023). Dado que los atributos ecofisiológicos se relacionan directamente con la adecuación de los organismos y modulan la respuesta de las poblaciones a los cambios ambientales, se ha abogado por su uso en ecología funcional (Rosado et al., 2013; Phillips et al., 2020; De Bello et al., 2021; Brandl et al., 2023). Aun así, las investigaciones sobre la variación en los atributos ecofisiológicos en ensamblajes de reptiles, y de animales en general, son escasas (Jiménez-Robles y De la Riva, 2019; S’khifa et al., 2020; Chown, 2023; Wiescher et al., 2012).
De acuerdo con Brandl y colaboradores (2023), los rasgos funcionales más frecuentemente usados en animales (e.g. talla corporal, dieta, movilidad, historias de vida, uso de hábitat) constituyen en última instancia facetas de la adquisición y asignación de energía por los organismos, por lo que plantean el uso de rasgos basados en tasas metabólicas para mejorar el entendimiento de los procesos de ensamblaje. Si bien la estimación de tasas metabólicas en ensamblajes animales no es aún tan común, el uso de atributos fisiológicos térmicos e hídricos ha permitido elucidar aspectos sobre el ensamblaje de comunidades de ectotermos (Wiescher et al., 2012; Phillips et al., 2020). En general, se reconoce que las especies pueden persistir en los ensamblajes locales solo si poseen rasgos funcionales compatibles con las condiciones específicas de su hábitat (Wiescher et al., 2012). En consecuencia, la variación en los atributos ecofisiológicos de las especies individuales determina la estructura funcional de los ensamblajes y sus posibles respuestas a las alteraciones ambientales (De Bello et al., 2021; Wiescher et al., 2012). En el caso de los reptiles, se ha documentado que solamente las especies más tolerantes al calor y a la deshidratación suelen persistir ante las modificaciones de su hábitat (Nowakowski et al., 2018a; Souza-Oliveira et al., 2024). Esto implica que las especies que no tienen la combinación de atributos ecofisiológicos necesaria para sobrellevar los cambios ambientales son filtradas de los ensamblajes (lo que modifica la estructura funcional inicial) (De Bello et al., 2021).
Además de la pérdida de especies, las modificaciones ambientales pueden conducir a cambios en la composición de los ensamblajes locales, en sus ámbitos de distribución y en sus interacciones (Lurgi et al., 2012). El aumento en la temperatura, ya sea por cambio climático o por pérdida de cobertura vegetal, podría permitir a especies adaptadas a temperaturas más cálidas y hábitats abiertos invadir el hábitat de especies de bosque, las cuales suelen presentar intervalos de tolerancia térmica más estrechos y termorregular menos eficientemente (Huey et al., 2009; Souza-Oliveira et al., 2024). En latitudes tropicales, donde las montañas son un factor de aislamiento más fuerte debido a la menor oscilación térmica y donde las tolerancias térmicas de los organismos son más bajas (hipótesis Janzen) (Muñoz y Bodensteiner, 2019), esta reestructuración de los ensamblajes podría tener consecuencias más marcadas, ya que los regímenes térmicos a altas elevaciones ya no serían una barrera para el intercambio de especies. De igual manera, se ha sugerido que la modificación de los hábitats y el cambio climático podría favorecer el establecimiento de especies introducidas, las cuales podrían convertirse en invasoras y desplazar a las especies nativas debido a su mayor tolerancia fisiológica al disturbio (Kelley, 2014). Sin embargo, algunos estudios han mostrado que las diferencias fisiológicas entre especies nativas y no nativas pueden promover la división espacial (i.e. microhábitat) y temporal (i.e. horario de actividad) y permitir así su coexistencia (Romero-Báez et al., 2020; Ryan y Gunderson, 2021).
Por otra parte, se ha documentado que el calentamiento climático actual está ocasionando una disminución en la talla corporal de algunos ectotermos (Ohlberger, 2013; Riemer et al., 2018). Si bien, en condiciones normales, las altas temperaturas incrementan las tasas metabólicas, y por lo tanto el crecimiento, llega un punto en el que esta relación se invierte debido al déficit energético y de suministro de oxígeno que generan (Pörtner, 2002; Riemer et al., 2018). Cuando las disminuciones en talla son consistentes a través de las poblaciones de las distintas especies (ya sea por la reducción en talla de los individuos o por cambios en las abundancias relativas de las diferentes categorías etarias de la población), la talla corporal media a nivel ensamblaje también se ve afectada. Además, procesos como la migración y la extinción pueden también modificar la distribución de tallas del ensamblaje (Ohlberger, 2013). Dado que la talla corporal determina interacciones interespecíficas como la competencia y la depredación, se espera que el cambio climático modifique las cascadas tróficas y la estructura de tallas de las comunidades (Ohlberger, 2013; Riemer et al., 2018).
Aproximaciones mecanicistas para el modelado del riesgo de extinción
En las últimas tres décadas, los estudios enfocados en desarrollar, mejorar y aplicar los modelos de nicho ecológico (MNE) han proliferado (Santini et al., 2021; Sillero et al., 2021). Uno de los usos más comunes de los MNE, y particularmente de los modelos de distribución de especies, es el de estimar los cambios en la distribución de los taxones y su riesgo de extinción debido al cambio climático y a la deforestación (Fagundes et al., 2018; Santini et al., 2021). La mayoría de estos estudios parten de un enfoque correlativo (fenomenológico), caracterizado por la búsqueda de patrones de asociación estadística entre datos de presencia o abundancia de las especies e información ambiental, pero sin indagar a priori en los mecanismos responsables de dicha asociación (Dormann et al., 2012). Menos recurridos son los modelos mecanicistas (también conocidos como modelos basados en procesos), los cuales incluyen de manera explícita rasgos funcionales de las especies (e.g. morfológicos, fisiológicos, conductuales), mientras que consideran la presencia o abundancia de las especies como consecuencia emergente o indirecta de procesos ecológicos subyacentes (Dormann et al., 2012). Un tercer tipo de modelos, los híbridos, integran tanto información de distribución de las especies, para la calibración de parámetros, como conocimiento ecológico previo, de manera que este tipo de modelos yace en un punto medio del continuo correlativo-mecanicista (Dormann et al., 2012).
Si bien ninguno de los tres tipos de modelos es inherentemente superior a los demás, el uso de cada uno de ellos supone tanto ventajas como desventajas (Dormann et al., 2012). Al incorporar explícitamente procesos y rasgos funcionales, los modelos mecanicistas 1) reducen el riesgo de extrapolación bajo nuevas condiciones ambientales (al proyectar en tiempo y espacio); 2) permiten modelar los procesos mismos que determinan la distribución de las especies, y 3) hacen posible considerar la variación geográfica en los rasgos, la plasticidad fenotípica y la adaptación (Enriquez-Urzelai et al., 2020; Sillero et al., 2021). No obstante, este tipo de modelos suele requerir una gran cantidad de información sobre los rasgos de las especies e información ambiental en alta resolución espacio-temporal (Dormann et al., 2012; Sillero et al., 2021). Debido a esto, los estudios con enfoque mecanicista, incluso aquellos de tipo híbrido, son aún relativamente escasos (Winter et al., 2016; Hayden-Bofill y Blom, 2024). Afortunadamente, cada vez existen más bases de datos (e.g. SquamEWL (Le Galliard et al., 2021); ReptTraits, (Oskyrko et al., 2024)) y código de acceso abierto (e.g. NicheMapR, (Kearney y Porter, 2017, 2020)); TrenchR, (Buckley et al., 2023); Mapinguari, (Caetano et al., 2017)) que facilitan la construcción de MNE mecanicistas.
Los MNE mecanicistas se basan en gran medida en los principios de la ecología biofísica, particularmente en aspectos de flujo y balance de masa y energía (i.e. agua, alimento y calor) (Kearney y Porter, 2009; Briscoe et al., 2023) (por ello, los términos modelo mecanicista y modelo biofísico suelen ser usados de manera sinónima en la literatura (Peterson et al., 2015)). Al basarse en principios físicos universales, estos modelos pueden ser usados para inferir lo que podría suceder bajo cualquier combinación de rasgos funcionales y condiciones ambientales (Briscoe et al., 2023). En el contexto de los cambios ambientales, esto supone una gran ventaja sobre los modelos correlativos, cuya capacidad para estimar condiciones nuevas puede verse mermada debido a la falta de observaciones bajo tales condiciones para parametrizar los modelos (Briscoe et al., 2023). La parametrización de los MNE mecanicistas, por su parte, depende de datos empíricos obtenidos a partir de experimentos u observaciones fisiológicas, conductuales y morfológicas de los organismos, tales como sus tasas metabólicas, aspectos de balance hídrico, límites térmicos, talla y forma corporal, propiedades físicas de la piel y comportamiento (Riddell et al., 2023).
Los modelos mecanicistas han sido empleados exitosamente para estimar el riesgo de extinción de algunas especies de reptiles bajo diferentes escenarios de cambio climático y de pérdida de cobertura vegetal (Sinervo et al., 2010; Muñoz-Nolasco et al., 2023; Lara-Reséndiz et al., 2024). Al incorporar de manera explícita parámetros fisiológicos, morfológicos y conductuales de los organismos, estos modelos han permitido relacionar dichos atributos con la distribución, actividad y vulnerabilidad de algunos taxones a los cambios en su ambiente físico (Sinervo et al., 2010; Caetano et al., 2020; Mader et al., 2022; Lara-Reséndiz et al., 2024). Más aún, la integración de la teoría del presupuesto energético dinámico (dynamic energy budget theory; (Kooijman, 2009)) en modelos mecanicistas ha posibilitado la construcción de modelos más precisos, acotados a diferentes estados y estadios del ciclo de vida de los organismos (Kearney y Porter, 2020). Por ello, se ha propuesto usar herramientas de modelado mecanicista para evaluar las áreas idóneas para la translocación de especies como medida de conservación ante el cambio climático (Sinervo et al., 2024), considerando no solo la fisiología de los organismos adultos, sino también los límites térmicos para el desarrollo embrionario (Mitchell et al., 2016). Debido al potencial de los MNE mecanicistas para guiar decisiones de conservación, algunos autores han hecho el llamado a la colaboración entre fisiólogos, especialistas en modelos de nicho y conservacionistas para el desarrollo de modelos más precisos y estrategias de conservación adecuadas a fin de hacer frente a los cambios ambientales (Evans et al., 2015).
Conclusiones y perspectivas emergentes
La comprensión de las posibles respuestas ecofisiológicas de los reptiles a los cambios ambientales es crucial para evaluar su vulnerabilidad y diseñar estrategias de conservación efectivas (Tracy et al., 2006; Nowakowski et al., 2018a; Lara-Reséndiz et al., 2024). Las alteraciones en las condiciones físicas del ambiente, inducidas tanto por el cambio climático como por el cambio de uso de suelo, conllevan afectaciones en la fisiología térmica e hídrica de estos organismos, las cuales pueden impactar negativamente en su adecuación y conducir al colapso poblacional (Tracy et al., 2006; Sinervo et al., 2010; Nowakowski et al., 2018a). Los avances más recientes en el estudio de la ecofisiología de este y otros grupos de ectotermos han subrayado la importancia de incorporar aproximaciones funcionales y mecanicistas a fin de proporcionar una visión más precisa de las consecuencias de las modificaciones ambientales sobre los organismos a nivel intra- e interespecífico (Rosado et al., 2013; Evans et al., 2015). No obstante, existen aún áreas de investigación que requieren mayor atención o que, francamente, han sido pobremente exploradas.
Por ejemplo, la mayoría de las evaluaciones de vulnerabilidad en reptiles han sido realizadas con base en organismos adultos, mientras que otras etapas de la ontogenia, particularmente el desarrollo embrionario, han sido menos estudiadas en comparación (Mitchell et al., 2016; Hall y Warner, 2018). Más allá de la mortalidad en etapas tempranas del desarrollo, se ha sugerido que el incremento en las temperaturas podría también tener efectos adversos sobre el funcionamiento neuronal y cognitivo en reptiles y otros ectotermos (Beltrán et al., 2021). Del mismo modo, se desconocen los límites térmicos de fertilidad para la gran mayoría de los taxones, esto a pesar de que los efectos subletales de las altas temperaturas a nivel reproductor podrían impactar a las poblaciones con mayor fuerza que los efectos letales por sobrecalentamiento (Quintero-Pérez et al., 2023; Bretman et al., 2024). Esto subraya la importancia de incorporar aspectos de sensibilidad térmica en función de la ontogenia y de la maduración espermática en modelos híbridos y mecanicistas, lo que podría incrementar su poder predictivo y precisión. Por otra parte, el conocimiento acerca de los mecanismos epigenéticos que median los efectos de la temperatura en reptiles es prácticamente nulo, lo cual es preocupante si se considera que la temperatura afecta la metilación del DNA a nivel del genoma completo en muchos animales (Singh et al., 2020). Menos aún es lo que se sabe acerca de los efectos a nivel epigenético y fenotípico de la restricción hídrica (Dupoué et al., 2019), y en general los aspectos de hidrorregulación han sido mucho menos estudiados en reptiles que aquellos relacionados con la termorregulación y los límites térmicos (Pirtle et al., 2019).
Esta brecha de conocimiento se extiende al ambiente físico del nido, el cual modula directamente el éxito del desarrollo. Nuestra comprensión acerca de los efectos de los cambios ambientales sobre la anidación en reptiles está limitada a algunos pocos taxones en los que este comportamiento es fácilmente observable, como tortugas y cocodrilos (Du et al., 2023). Dado que los huevos mantienen su balance hídrico al absorber agua del suelo, y considerando las limitadas capacidades de termorregulación del embrión dentro del huevo, documentar los cambios térmicos e hídricos inducidos por las modificaciones ambientales en los nidos representa una tarea prioritaria. Para especies vivíparas el reto no es menos urgente, puesto que las hembras gestantes tienden a ser más vulnerables a los efectos de la deshidratación y de la hipertermia que los machos y las hembras no grávidas (Lourdais et al., 2017; Virens y Cree, 2019). Es por ello por lo que hacen falta más estudios que aborden las consecuencias ecológicas y evolutivas de las respuestas maternas a las alteraciones térmicas e hídricas.
Otro factor crítico que introduce incertidumbre en las proyecciones de riesgo es la adaptación local. En la mayoría de los casos, se dispone de muy pocos datos sobre la variación intraespecífica de los atributos fisiológicos, sean térmicos o hídricos, en la misma especie a través de diferentes ambientes (Buckley et al., 2015; Belasen et al., 2017; Pontes-da-Silva et al., 2018). Esta carencia de información puede sesgar la inferencia sobre el nicho fundamental de una determinada especie y, por lo tanto, llevar a una sobreestimación o subestimación de su capacidad real de adaptación al cambio climático. Finalmente, para evaluar la viabilidad poblacional a largo plazo, también se requiere un mejor entendimiento de la tasa de cambio evolutivo de estos rasgos en respuesta a las presiones ambientales, un área que permanece en gran medida inexplorada, salvo contadas excepciones (Bodensteiner et al., 2021).
A pesar del potencial de los enfoques mecanicistas, la ecofisiología de reptiles enfrenta una limitante crítica: la falta de estudios de repetibilidad y estandarización (Taylor et al., 2021). Gran parte de la evidencia que sustenta las predicciones sobre vulnerabilidad y riesgo de extinción se enmarca en trabajos aislados y con metodologías diversas (Caetano et al., 2020; Arenas-Moreno et al., 2021; Briscoe et al., 2023). Esta heterogeneidad dificulta la comparación robusta de resultados entre especies y poblaciones y, lo que es más importante, la síntesis de datos para construir modelos predictivos a gran escala. Para superar esta limitación, es imperativo que la comunidad científica adopte la estandarización de protocolos para la medición de rasgos fisiológicos funcionales y promueva la replicación sistemática para construir bases de datos con la variación ambiental e intraespecífica necesaria para calibrar modelos mecanicistas fiables (Le Galliard et al., 2021; Oskyrko et al., 2024).
Las consecuencias de las modificaciones ambientales sobre los ensamblajes de reptiles a nivel ecofisiológico son igualmente poco conocidas. Se sabe, sin embargo, que la heterogeneidad microclimática es uno de los factores que determinan la variación ecofisiológica y la composición de los ensamblajes de reptiles a través del paisaje (Jiménez-Robles y de la Riva, 2019). Esto plantea la posibilidad de emplear modelos que incorporen parámetros microclimáticos y ecofisiológicos para determinar patrones de riesgo de extinción en ensamblajes de reptiles y de otros ectotermos, lo que mejoraría el entendimiento de la interacción entre cambio climático y cambio de uso de suelo y contribuiría a forjar mejores estrategias de conservación (Nowakowski et al., 2018b). Asimismo, a fin de estimar de manera más precisa los impactos de las alteraciones ambientales, es necesario considerar las interacciones bióticas, pues estas pueden limitar el nicho fundamental de las especies y determinar su nicho realizado (Riddell et al., 2023). El reto reside en integrar estos conocimientos en modelos predictivos que consideren la complejidad de las interacciones entre los diferentes factores del cambio global. Esto permitirá una mejor estimación de la vulnerabilidad de los reptiles a las alteraciones antrópicas, así como un manejo más adecuado de sus hábitats en pos de asegurar la conservación de sus poblaciones y de sus ensamblajes en un mundo en constante cambio.
Contribución de los autores
Francisco Javier Muñoz-Nolasco: Conceptualization, Investigation, Writing – original draft. Víctor L. Barradas: Supervision, Validation, Writing – review & editing. Andrés García: Supervision, Validation, Writing – review & editing. Fausto R. Méndez de la Cruz: Supervision, Validation, Writing – review & editing.
Disponibilidad de datos y código
No se utilizaron conjuntos de datos ni código para la elaboración de este artículo.
Financiación, permisos requeridos, potenciales conflictos de interés y agradecimientos
Este proyecto contó con el auspicio del Programa de Apoyo a Proyectos de Investigación e Innovación Tecnológica (Papiit) con los proyectos IN208624 e IN212724. FJMN recibió una beca doctoral por parte de la Secretaría de Ciencia, Humanidades, Tecnología e Innovación (Secihti; CVU 775920).
Los autores/as declaran no tener ningún conflicto de intereses.
Los autores agradecemos a Mirna Crizel Vera-Chávez por facilitar las fotografías de la Figura 3.
Referencias
Amiel, J. J., & Shine12, R. (2012). Hotter nests produce smarter young lizards. Biology Letters, 8, 372–374. https://doi.org/10.1098/rsbl.2011.1161
Angilletta, M. J., Jr., Bennett, A. F., Guderley, H., Navas, C. A., Seebacher, F., & Wilson, R. S. (2006). Coadaptation: A unifying principle in evolutionary thermal biology. Physiological and Biochemical Zoology, 79, 282–294. https://doi.org/10.1086/499990
Arenas-Moreno, D. M., Lara-Reséndiz, R. A., Domínguez-Guerrero, S. F., Pérez-Delgadillo, A. G., Muñoz-Nolasco, F. J., Galina-Tessaro, P., & Méndez-de la Cruz, F. R. (2021). Thermoregulatory strategies of three reclusive lizards (genus Xantusia) from the Baja California peninsula, Mexico, under current and future microenvironmental temperatures. Journal of Experimental Zoology Part A: Ecological and Integrative Physiology, 335, 499–511. https://doi.org/10.1002/jez.2470
Battey, C. J., Otero, L. M., Gorman, G. C., Hertz, P. E., Lister, B. C., García, A., … Huey, R. B. (2019). Why montane Anolis lizards are moving downhill while Puerto Rico warms. bioRxiv, 751941. https://doi.org/10.1101/751941
Belasen, A., Brock, K., Li, B., Chremou, D., Valakos, E., Pafilis, P., Sinervo, B., & Foufopoulos, J. (2017). Fine with heat, problems with water: Microclimate alters water loss in a thermally adapted insular lizard. Oikos, 126, 447–457. https://doi.org/10.1111/oik.03712
Beltrán, I., Perry, C., Degottex, F., & Whiting, M. (2021). Behavioral thermoregulation by mothers protects offspring from global warming, but at a cost. Physiological and Biochemical Zoology, 94, 302–318. https://doi.org/10.1086/715976
Blois, J. L., Zarnetske, P. L., Fitzpatrick, M. C., & Finnegan, S. (2013). Climate change and the past, present, and future of biotic interactions. Science, 341, 499–504. https://doi.org/10.1126/science.1237184
Bodensteiner, B. L., Agudelo‐Cantero, G. A., Arietta, A. Z. A., Gunderson, A. R., Muñoz, M. M., Refsnider, J. M., & Gangloff, E. J. (2021). Thermal adaptation revisited: How conserved are thermal traits of reptiles and amphibians? Journal of Experimental Zoology Part A: Ecological and Integrative Physiology, 335, 173–194. https://doi.org/10.1002/jez.2414
Böhm, M., Cook, D., Ma, H., Davidson, A. D., García, A., Tapley, B., Pearce-Kelly, P., & Carr, J. (2016). Hot and bothered: Using trait-based approaches to assess climate change vulnerability in reptiles. Biological Conservation, 204, 32–41. https://doi.org/10.1016/j.biocon.2016.06.002
Bonnet, X., Naulleau, G., & Shine, R. (2017). The evolutionary economics of embryonic-sac fluids in squamate reptiles. American Naturalist, 189, 333–344. https://doi.org/10.1086/690119
Brandl, S. J., Lefcheck, J. S., Bates, A. E., Rasher, D. B., & Norin, T. (2023). Can metabolic traits explain animal community assembly and functioning? Biological Reviews, 98, 1–18. https://doi.org/10.1111/brv.12892
Bretman, A., Fricke, C., Baur, J., Berger, D., Breedveld, M. C., Dierick, D., … Snook, R. R. (2024). Systematic approaches to assessing high-temperature limits to fertility in animals. Journal of Evolutionary Biology, 37, 471–485. https://doi.org/10.1093/jeb/voae021
Briscoe, N. J., Morris, S. D., Mathewson, P. D., Buckley, L. B., Jusup, M., Levy, O., … Kearnwy, M. R. (2023). Mechanistic forecasts of species responses to climate change: The promise of biophysical ecology. Global Change Biology, 29, 1451–1470. https://doi.org/10.1111/gcb.16557
Buckley, L. B., Ehrenberger, J. C., & Angilletta, M. J. (2015). Thermoregulatory behaviour limits local adaptation of thermal niches and confers sensitivity to climate change. Functional Ecology, 29, 1038–1047. https://doi.org/10.1111/1365-2435.12406
Buckley, L., Briones Ortiz, B., Caruso, I., John, A., Levy, O., Meyer, A., … Simonis. J. L. (2023). TrenchR: An R package for modular and accessible microclimate and biophysical ecology. PLoS Climate, 2, e0000139. https://doi.org/10.1371/journal.pclm.0000139
Caetano, G., Santos, S., & Sinervo, B. (2017). Mapinguari. https://cran.r-project.org/web/packages/Mapinguari/index.html
Caetano, G. H. O., Santos, J. C., Godinho, L. B., Cavalcante, V. H. G. L., Diele-Viegas, L. M., Campelo, P. H., … Sinervo, B. R. (2020). Time of activity is a better predictor of the distribution of a tropical lizard than pure environmental temperatures. Oikos, 129, 953–963. https://doi.org/10.1111/oik.07123
Camacho, A., Angilletta, M. J., & Levy, O. (2023). A theoretical thermal tolerance function for ectothermic animals and its implications for identifying thermal vulnerability across large geographic scales. Diversity, 15, 680. https://doi.org/10.3390/d15050680
Charruau, P., Thorbjarnarson, J. B., & Hénaut, Y. (2010). Tropical cyclones and reproductive ecology of Crocodylus acutus Cuvier, 1807 (Reptilia: Crocodilia: Crocodylidae) on a Caribbean atoll in Mexico. Journal of Natural History, 44, 741–761. https://doi.org/10.1080/00222930903490993
Chen, Y.-H., Lenoir, J., & Chen, I.-C. (2025). Limited evidence for range shift–driven extinction in mountain biota. Science, 388, 741–747. https://doi.org/10.1126/science.adq9512
Chichorro, F., Urbano, F., Teixeira, D., Väre, H., Pinto, T., Brummitt, N., … Cardoso, P. (2022). Trait-based prediction of extinction risk across terrestrial taxa. Biological Conservation, 274, 109738. https://doi.org/10.1016/j.biocon.2022.109738
Chown, S. L. (2023). Macrophysiology for decision‐making. Journal of Zoology, 319, 1–22. https://doi.org/10.1111/jzo.13029
Cooke, S. J., Blumstein, D. T., Buchholz, R., Caro, T., Fernández-Juricic, E., Franklin, C. E., … Wikelski, M. (2014). Physiology, behavior, and conservation. Physiological and Biochemical Zoology, 87, 1–14. https://doi.org/10.1086/671165
Cordier, J. M., Aguilar, R., Lescano, J. N., Leynaud, G. C., Bonino, A., Miloch, D., Loyola, R., & Nori, J. (2021). A global assessment of amphibian and reptile responses to land-use changes. Biological Conservation, 253, 108863. https://doi.org/10.1016/j.biocon.2020.108863
Cornejo-Páramo, P., Lira-Noriega, A., Ramírez-Suástegui, C., Méndez-de-la-Cruz, F. R., Székely, T., Urrutia, A. O., & Cortez, D. (2020). Sex determination systems in reptiles are related to ambient temperature but not to the level of climatic fluctuation. BMC Evolutionary Biology, 20, 103. https://doi.org/10.1186/s12862-020-01671-y
Dai, A., Zhao, T., & Chen, J. (2018). Climate change and drought: A precipitation and evaporation perspective. Current Climate Change Reports, 4, 301–312. https://doi.org/10.1007/s40641-018-0101-6
De Bello, F., Carmona, C. P., Dias, A. T. C., Götzenberger, L., Moretti, M., & Berg, M. P. (Eds.). (2021). Handbook of trait-based ecology: From theory to R tools. Cambridge University Press.
Deutsch, C. A., Tewksbury, J. J., Huey, R. B., Sheldon, K. S., Ghalambor, C. K., Haak, D. C., & Martin, P. R. (2008). Impacts of climate warming on terrestrial ectotherms across latitude. Proceedings of the National Academy of Sciences of the United States of America, 105, 6668–6672. https://doi.org/10.1073/pnas.0709472105
Dezetter, M., Le Galliard, J. F., Guiller, G., Guillon, M., Leroux-Coyau, M., Meylan, S., … Lourdais, O. (2021). Water deprivation compromises maternal physiology and reproductive success in a cold and wet adapted snake Vipera berus. Conservation Physiology, 9, coab071. https://doi.org/10.1093/conphys/coab071
Domínguez-Guerrero, S. F., Méndez-de la Cruz, F. R., Manríquez-Morán, N. L., Olson, M. E., Galina-Tessaro, P., Arenas-Moreno, D. M., … Muñóz. M. M. (2022). Exceptional parallelisms characterize the evolutionary transition to live birth in phrynosomatid lizards. Nature Communications, 13, 2881. https://doi.org/10.1038/s41467-022-30535-w
Dormann, C. F., Schymanski, S. J., Cabral, J., Chuine, I., Graham, C., Hartig, F., … Singer, A. (2012). Correlation and process in species distribution models: Bridging a dichotomy. Journal of Biogeography, 39, 2119–2131. https://doi.org/10.1111/j.1365-2699.2011.02659.x
Du, W., & Shine, R. (2015). The behavioural and physiological strategies of bird and reptile embryos in response to unpredictable variation in nest temperature. Biological Reviews, 90, 19–30. https://doi.org/10.1111/brv.12089
Du, W.-G., Li, S.-R., Sun, B.-J., & Shine, R. (2023). Can nesting behaviour allow reptiles to adapt to climate change? Philosophical Transactions of the Royal Society B: Biological Sciences, 378, 20220153. https://doi.org/10.1098/rstb.2022.0153
Dupoué, A., Lourdais, O., Meylan, S., Brischoux, F., Angelier, F., Rozen-Rechels, D., … Le Galliard, J.-F. (2019). Some like it dry: Water restriction overrides heterogametic sex determination in two reptiles. Ecology and Evolution, 9, 6524–6533. https://doi.org/10.1002/ece3.5229
Dupoué, A., Sorlin, M., Richard, M., Galliard, J. L., Lourdais, O., Clobert, J., & Aubret, F. (2020). Mother–offspring conflict for water and its mitigation in the oviparous form of the reproductively bimodal lizard Zootoca vivipara. Biological Journal of the Linnean Society, 129, 888–900. https://doi.org/10.1093/biolinnean/blaa012
Endler, J., & Basolo, A. L. (1998). Sensory ecology, receiver biases and sexual selection. Trends in Ecology & Evolution, 13, 415–420. https://doi.org/10.1016/S0169-5347(98)01471-2
Enriquez-Urzelai, U., Tingley, R., Kearney, M. R., Sacco, M., Palacio, A. S., Tejedo, M., & Nicieza, A. G. (2020). The roles of acclimation and behaviour in buffering climate change impacts along elevational gradients. Journal of Animal Ecology, 89, 1722–1734. https://doi.org/10.1111/1365-2656.13222
Evans, T. G., Diamond, S. E., & Kelly, M. W. (2015). Mechanistic species distribution modelling as a link between physiology and conservation. Conservation Physiology, 3, cov056. https://doi.org/10.1093/conphys/cov056
Fagundes, C. K., Vogt, R. C., De Souza, R. A., & De Marco, P., Jr. (2018). Vulnerability of turtles to deforestation in the Brazilian Amazon: Indicating priority areas for conservation. Biological Conservation, 226, 300–310. https://doi.org/10.1016/j.biocon.2018.08.009
Farooq, H., Harfoot, M., Rahbek, C., & Geldmann, J. (2024). Threats to reptiles at global and regional scales. Current Biology, 34, 2231–2237.e2. https://doi.org/10.1016/j.cub.2024.04.007
Feldmeier, S., Schmidt, B. R., Zimmermann, N. E., Veith, M., Ficetola, G. F., & Lötters, S. (2020). Shifting aspect or elevation? The climate change response of ectotherms in a complex mountain topography. Diversity and Distributions, 26, 1483–1495. https://doi.org/10.1111/ddi.13146
Ferreira, D., Mateus, C., & Santos, X. (2016). Responses of reptiles to fire in transition zones are mediated by bioregion affinity of species. Biodiversity and Conservation, 25, 1543–1557. https://doi.org/10.1007/s10531-016-1137-3
Fitzgerald, L. A., Walkup, D., Chyn, K., Buchholtz, E., Angeli, N., & Parker, M. (2018). The future for reptiles: Advances and challenges in the Anthropocene. In D. DellaSala & M. Goldstein (Eds.), Encyclopedia of the Anthropocene (pp. 163–174). Elsevier Science Ltd.
Foucart, T., Heulin, B., & Lourdais, O. (2018). Small changes, big benefits: Testing the significance of maternal thermoregulation in a lizard with extended egg retention. Biological Journal of the Linnean Society, 125, 280–291. https://doi.org/10.1093/biolinnean/bly105
Freeman, B. G., Lee‐Yaw, J. A., Sunday, J. M., & Hargreaves, A. L. (2018). Expanding, shifting and shrinking: The impact of global warming on species’ elevational distributions. Global Ecology and Biogeography, 27, 1268–1276. https://doi.org/10.1111/geb.12774
Frishkoff, L. O., Hadly, E. A., & Daily, G. C. (2015). Thermal niche predicts tolerance to habitat conversion in tropical amphibians and reptiles. Global Change Biology, 21, 3901–3916. https://doi.org/10.1111/gcb.13016
Gangloff, E. J., Sorlin, M., Cordero, G. A., Souchet, J., & Aubret, F. (2019). Lizards at the peak: Physiological plasticity does not maintain performance in lizards transplanted to high altitude. Physiological and Biochemical Zoology, 92, 189–200. https://doi.org/10.1086/701793
García, R. A., & Clusella-Trullas, S. (2019). Thermal landscape change as a driver of ectotherm responses to plant invasions. Proceedings of the Royal Society B: Biological Sciences, 286, 20191020. https://doi.org/10.1098/rspb.2019.1020
Griffis-Kyle, K. L., Mougey, K., Vanlandeghem, M., Swain, S., & Drake, J. C. (2018). Comparison of climate vulnerability among desert herpetofauna. Biological Conservation, 225, 164–165. https://doi.org/10.1016/j.biocon.2018.06.009
Grossiord, C., Buckley, T. N., Cernusak, L. A., Novick, K. A., Poulter, B., Siegwolf, R. T. W., … McDowell, N. G. (2020). Plant responses to rising vapor pressure deficit. New Phytologist, 226, 1550–1566. https://doi.org/10.1111/nph.16485
Habibullah, M. S., Din, B. H., Tan, S.-H., & Zahid, H. (2022). Impact of climate change on biodiversity loss: Global evidence. Environmental Science and Pollution Research, 29, 1073–1086. https://doi.org/10.1007/s11356-021-15702-8
Hall, J. M., & Warner, D. A. (2018). Thermal spikes from the urban heat island increase mortality and alter physiology of lizard embryos. Journal of Experimental Biology, 221, jeb181552. https://doi.org/10.1242/jeb.181552
Hayden-Bofill, S. I., & Blom, M. P. K. (2024). Climate change from an ectotherm perspective: Evolutionary consequences and demographic change in amphibian and reptilian populations. Biodiversity and Conservation, 33, 905–927. https://doi.org/10.1007/s10531-023-02772-y
Huey, R. B., Deutsch, C. A., Tewksbury, J. J., Vitt, L. J., Hertz, P. E., Álvarez Pérez, H. J., & Garland, T., Jr. (2009). Why tropical forest lizards are vulnerable to climate warming. Proceedings of the Royal Society B: Biological Sciences, 276, 1939–1948. https://doi.org/10.1098/rspb.2008.1957
Huey, R. B., Losos, J. B., & Moritz, C. (2010). Are lizards toast? Science, 328(5980), 832-833. https://doi.org/10.1126/science.1190374
Huey, R. B., Kearney, M. R., Krockenberger, A., Holtum, J. A. M., Jess, M., & Williams, S. E. (2012). Predicting organismal vulnerability to climate warming: Roles of behaviour, physiology and adaptation. Philosophical Transactions of the Royal Society B: Biological Sciences, 367, 1665–1679. https://doi.org/10.1098/rstb.2012.0005
Jaureguiberry, P., Titeux, N., Wiemers, M., Bowler, D. E., Coscieme, L., Golden, A. S., … Purvis, A. (2022). The direct drivers of recent global anthropogenic biodiversity loss. Science Advances, 8, eabm9982. https://doi.org/10.1126/sciadv.abm9982
Jiménez-Robles, O., & de la Riva, I. (2019). Lizards in the mist: Thermal niches constrained by habitat and microclimates in the Andes of southern Bolivia. Journal of Biogeography, 46, 1676–1686. https://doi.org/10.1111/jbi.13660
Kearney, R. M. (2013). Activity restriction and the mechanistic basis for extinctions under climate warming. Ecology Letters, 16, 1470–1479. https://doi.org/10.1111/ele.12192
Kearney, M., & Porter, W. (2009). Mechanistic niche modelling: Combining physiological and spatial data to predict species’ ranges. Ecology Letters, 12, 334–350. https://doi.org/10.1111/j.1461-0248.2008.01277.x
Kearney, M. R., & Porter, W. P. (2017). NicheMapR – An R package for biophysical modelling: The microclimate model. Ecography, 40, 664–674. https://doi.org/10.1111/ecog.02360
Kearney, M. R., & Porter, W. P. (2020). NicheMapR – An R package for biophysical modelling: The ectotherm and Dynamic Energy Budget models. Ecography, 43, 85–96. https://doi.org/10.1111/ecog.04680
Keinath, D. A., Doak, D. F., Hodges, K. E., Prugh, L. R., Fagan, W., Sekercioglu, C. H., Buchart, S. H. M., & Kauffman, M. (2017). A global analysis of traits predicting species sensitivity to habitat fragmentation. Global Ecology and Biogeography, 26, 115–127. https://doi.org/10.1111/geb.12509
Kelley, A. L. (2014). The role thermal physiology plays in species invasion. Conservation Physiology, 2, cou045. https://doi.org/10.1093/conphys/cou045
Kooijman, B. (2009). Dynamic Energy Budget Theory for Metabolic Organisation (3rd ed.). Cambridge University Press.
Lara-Reséndiz, R. A., Álvarez-Yepiz, J. C., Miles, D. B., Joos, J., Pérez-Delgadillo, A. G., & Méndez-de la Cruz, F. R. (2024). Climate change and reduced shading restrict the activity period of a threatened tortoise in tropical dry forest. Global Ecology and Conservation, 50, e02841. https://doi.org/10.1016/j.gecco.2024.e02841
Le Galliard, J.-F., Chabaud, C., de Andrade, D. O. V., Brischoux, F., Carretero, M. A., Dupoué, A., … Van Dooren, T. J. M. (2021). SquamEWL: A worldwide and annotated database of evaporative water loss rates in squamate reptiles. Global Ecology and Biogeography, 30, 1938–1950. https://doi.org/10.1111/geb.13355
Lillywhite, H. B. (2016). Behavior and physiology: An ecological and evolutionary viewpoint on the energy and water relations of ectothermic amphibians and reptiles. In Amphibian and reptile adaptations to the environment: Interplay between physiology and behavior (pp. 1–39). CRC Press.
Loughran, C. L., & Wolf, B. O. (2020). The functional significance of panting as a mechanism of thermoregulation and its relationship to the critical thermal maxima in lizards. Journal of Experimental Biology, 223, jeb224139. https://doi.org/10.1242/jeb.224139
Lourdais, O., Dupoué, A., Guillon, M., Guiller, G., Michaud, B., & DeNardo, D. F. (2017). Hydric “costs” of reproduction: Pregnancy increases evaporative water loss in the snake Vipera aspis. Physiological and Biochemical Zoology, 90, 663–672. https://doi.org/10.1086/694848
Lurgi, M., López, B. C., & Montoya, J. M. (2012). Novel communities from climate change. Philosophical Transactions of the Royal Society B: Biological Sciences, 367, 2913–2922. https://doi.org/10.1098/rstb.2012.0238
Mader, S., Goldenberg, J., Massetti, F., Bisschop, K., D’Alba, L., Etienne, R. S., Clusella-Trullas, S., & Shawkey, M. D. (2022). How melanism affects the sensitivity of lizards to climate change. Functional Ecology, 36, 812–825. https://doi.org/10.1111/1365-2435.13993
Martín, J., & López, P. (2013). Effects of global warming on sensory ecology of rock lizards: Increased temperatures alter the efficacy of sexual chemical signals. Functional Ecology, 27, 1332–1340. https://doi.org/10.1111/1365-2435.12128
Mitchell, N. J., Rodriguez, N., Kuchling, G., Arnall, S. G., & Kearney, M. R. (2016). Reptile embryos and climate change: Modelling limits of viability to inform translocation decisions. Biological Conservation, 204, 134–147. https://doi.org/10.1016/j.biocon.2016.04.004
Muñoz, M. M., & Bodensteiner, B. L. (2019). Janzen’s hypothesis meets the Bogert effect: Connecting climate variation, thermoregulatory behavior, and rates of physiological evolution. Integrative Organismal Biology, 1, oby002. https://doi.org/10.1093/iob/oby002
Muñoz-Nolasco, F. J., Arenas-Moreno, D. M., Santos-Bibiano, R., Bautista-del Moral, A., Gandarilla-Aizpuro, F. J., Brindis-Badillo, D. A., & Méndez-de la Cruz, F. R. (2019). Evaporative water loss of some habitat-restricted Mexican lizard species. Herpetological Conservation and Biology, 14, 51–66. https://www.herpconbio.org/Volume_14/Issue_1/Munoz-Nolasco_etal_2019.pdf
Muñoz-Nolasco, F. J., Arenas-Moreno, D. M., Gandarilla-Aizpuro, F. J., Bautista-del Moral, A., Santos-Bibiano, R., Miles, D. B., & Méndez-de la Cruz, F. R. (2023). Physiological ecology and vulnerability to climate change of a microendemic, habitat-specialist lizard in a tropical dry forest of Mexico. Climate Change Ecology, 5, 100066. https://doi.org/10.1016/j.ecochg.2023.100066
Murphy, M. S., & DeNardo, D. F. (2019). Rattlesnakes must drink: Meal consumption does not improve hydration state. Physiological and Biochemical Zoology, 92, 381–385. https://doi.org/10.1086/704081
Murray, K. A., Verde Arregoitia, L. D., Davidson, A., Di Marco, M., & Di Fonzo, M. M. I. (2014). Threat to the point: Improving the value of comparative extinction risk analysis for conservation action. Global Change Biology, 20, 483–494. https://doi.org/10.1111/gcb.12366
Noble, D. W. A., Stenhouse, V., & Schwanz, L. E. (2018). Developmental temperatures and phenotypic plasticity in reptiles: A systematic review and meta‐analysis. Biological Reviews, 93, 72–97. https://doi.org/10.1111/brv.12333
Nowakowski, A. J., Frishkoff, L. O., Agha, M., Todd, B. D., & Scheffers, B. R. (2018b). Changing thermal landscapes: Merging climate science and landscape ecology through thermal biology. Current Landscape Ecology Reports, 3, 57–72. https://doi.org/10.1007/s40823-018-0034-8
Nowakowski, A. J., Watling, J. I., Thompson, M. E., Brusch, G. A., Catenazzi, A., Whitfield, S. M., … Todd, B. D. (2018a). Thermal biology mediates responses of amphibians and reptiles to habitat modification. Ecology Letters, 21, 345–355. https://doi.org/10.1111/ele.12901
Ohlberger, J. (2013). Climate warming and ectotherm body size: From individual physiology to community ecology. Functional Ecology, 27, 991–1001. https://doi.org/10.1111/1365-2435.12098
Oskyrko, O., Mi, C., Meiri, S., & Du, W. (2024). ReptTraits: A comprehensive dataset of ecological traits in reptiles. Scientific Data, 11, 243. https://doi.org/10.1038/s41597-024-03079-5
Parratt, S. R., Walsh, B. S., Metelmann, S., White, N., Manser, A., Bretman, A. J., … Price, T. A. R. (2021). Temperatures that sterilize males better match global species distributions than lethal temperatures. Nature Climate Change, 11, 481–484. https://doi.org/10.1038/s41558-021-01047-0
Peterson, A. T., Papeş, M., & Soberón, J. (2015). Mechanistic and correlative models of ecological niches. European Journal of Ecology, 1, 28–38. https://doi.org/10.1515/eje-2015-0014
Phillips, L. M., Aitkenhead, I., Janion-Scheepers, C., King, C. K., McGeoch, M. A., Nielsen, U. N., … Chown, S. L. (2020). Basal tolerance but not plasticity gives invasive springtails the advantage in an assemblage setting. Conservation Physiology, 8, coaa049. https://doi.org/10.1093/conphys/coaa049
Pincheira‐Donoso, D., Tregenza, T., Witt, M. J., & Hodgson, D. J. (2013). The evolution of viviparity opens opportunities for lizard radiation but drives it into a climatic cul‐de‐sac. Global Ecology and Biogeography, 22, 857–867. https://doi.org/10.1111/geb.12052
Pirtle, E. I., Tracy, C. R., & Kearney, M. R. (2019). Hydroregulation: A neglected behavioral response of lizards to climate change? In Behavior of lizards: Evolutionary and mechanistic perspectives (pp. 343–374). CRC Press.
Plummer, M. V., Williams, B. K., Skiver, M. M., & Carlyle, J. C. (2003). Effects of dehydration on the critical thermal maximum of the Desert Box Turtle (Terrapene ornata luteola). Journal of Herpetology, 37, 747–750. https://doi.org/10.1670/18-03N
Pontes-da-Silva, E., Magnusson, W. E., Sinervo, B., Caetano, G. H., Miles, D. B., Colli, G. R., … Werneck, F. P. (2018). Extinction risks forced by climatic change and intraspecific variation in the thermal physiology of a tropical lizard. Journal of Thermal Biology, 73, 50–60. https://doi.org/10.1016/j.jtherbio.2018.01.013
Pörtner, H. O. (2002). Climate variations and the physiological basis of temperature-dependent biogeography: Systemic to molecular hierarchy of thermal tolerance in animals. Comparative Biochemistry and Physiology Part A: Molecular & Integrative Physiology, 132, 739–761. https://doi.org/10.1016/S1095-6433(02)00045-4
Quintero-Pérez, R. I., Méndez-de la Cruz, F. R., Miles, D. B., Vera Chávez, M. C., López-Ramírez, Y., Arenas-Moreno, D. M., & Arenas-Ríos, E. (2023). Trade-off between thermal preference and sperm maturation in a montane lizard. Journal of Thermal Biology, 113, 103526. https://doi.org/10.1016/j.jtherbio.2023.103526
Recknagel, H., Kamenos, N. A., & Elmer, K. R. (2018). Common lizards break Dollo’s law of irreversibility: Genome-wide phylogenomics support a single origin of viviparity and re-evolution of oviparity. Molecular Phylogenetics and Evolution, 127, 579–588. https://doi.org/10.1016/j.ympev.2018.05.029
Riddell, E. A., Burger, I. J., Tyner-Swanson, T. L., Biggerstaff, J., Muñoz, M. M., Levy, O., & Porter, C. K. (2023). Parameterizing mechanistic niche models in biophysical ecology: A review of empirical approaches. Journal of Experimental Biology, 226, jeb245543. https://doi.org/10.1242/jeb.245543
Riemer, K., Anderson‐Teixeira, K. J., Smith, F. A., Harris, D. J., & Ernest, S. K. M. (2018). Body size shifts influence effects of increasing temperatures on ectotherm metabolism. Global Ecology and Biogeography, 27, 958–967. https://doi.org/10.1111/geb.12757
Roberts, J. B., & Lillywhite, H. B. (1980). Lipid barrier to water exchange in reptile epidermis. Science, 207, 1077–1079. https://doi.org/10.1126/science.207.4435.1077
Romero-Báez, Ó., Santos-Bibiano, R., Domínguez-Godoy, M. A., & Miles, D. B. (2020). Thermal ecophysiology of a native and an invasive gecko species in a tropical dry forest of Mexico. Journal of Thermal Biology, 90, 102607. https://doi.org/10.1016/j.jtherbio.2020.102607
Rosado, B. H. P., Dias, A. T. C., & De Mattos, E. A. (2013). Going back to basics: Importance of ecophysiology when choosing functional traits for studying communities and ecosystems. Natureza & Conservação, 11, 15–22. https://doi.org/10.4322/NATCON.2013.002
Rozen-Rechels, D., Dupoué, A., Meylan, S., Decencière, B., Guingand, S., & Le Galliard, J.-F. (2018). Water restriction in viviparous lizards causes transgenerational effects on behavioral anxiety and immediate effects on exploration behavior. Behavioral Ecology and Sociobiology, 72, 23. https://doi.org/10.1007/s00265-018-2443-4
Rozen-Rechels, D., Dupoué, A., Lourdais, O., Chamaillé-Jammes, S., Meylan, S., Clobert, J., & Le Galliard, J.-F. (2019). When water interacts with temperature: Ecological and evolutionary implications of thermo-hydroregulation in terrestrial ectotherms. Ecology and Evolution, 9, 10029–10043. https://doi.org/10.1002/ece3.5440
Rubalcaba, J. G., & Olalla-Tárraga, M. Á. (2020). The biogeography of thermal risk for terrestrial ectotherms: Scaling of thermal tolerance with body size and latitude. Journal of Animal Ecology, 89, 1277–1285. https://doi.org/10.1111/1365-2656.13181
Ryan, L. M., & Gunderson, A. R. (2021). Competing native and invasive Anolis lizards exhibit thermal preference plasticity in opposite directions. Journal of Experimental Zoology Part A: Ecological and Integrative Physiology, 335, 118–125. https://doi.org/10.1002/jez.2420
Sannolo, M., & Carretero, M. A. (2019). Dehydration constrains thermoregulation and space use in lizards. PLoS ONE, 14, e0220384. https://doi.org/10.1371/journal.pone.0220384
Sannolo, M., Barroso, F. M., & Carretero, M. A. (2018). Physiological differences in preferred temperatures and evaporative water loss rates in two sympatric lacertid species. Zoology, 126, 58–64. https://doi.org/10.1016/j.zool.2017.12.003
Santidrián-Tomillo, P., & Spotila, J. R. (2020). Temperature-dependent sex determination in sea turtles in the context of climate change: Uncovering the adaptive significance. BioEssays, 42, 2000146. https://doi.org/10.1002/bies.202000146
Santini, L., Benítez-López, A., Maiorano, L., Čengić, M., & Huijbregts, M. A. J. (2021). Assessing the reliability of species distribution projections in climate change research. Diversity and Distributions, 27, 1035–1050. https://doi.org/10.1111/ddi.13252
Schwarzkopf, L. (2022). Homage to reptiles and amphibians as model systems: One ecologist’s view. Journal of Herpetology, 56, 45–55. https://doi.org/10.1670/21-020
Senior, A. F., Böhm, M., Johnstone, C. P., McGee, M. D., Meiri, S., Chapple, D. G., & Tingley, R. (2021). Correlates of extinction risk in Australian squamate reptiles. Journal of Biogeography, 48, 2144–2152. https://doi.org/10.1111/jbi.14140
Serén, N., Pinho, C., Megía-Palma, R., Aguilar, P., Žagar, A., Andrade, P., & Carretero, M. A. (2025). Selection on the vascular-remodeling BMPER gene is associated with altitudinal adaptation in an insular lizard. Evolution Letters, 9, 41–50. https://doi.org/10.1093/evlett/qrae047
Shivanna, K. R. (2022). Climate change and its impact on biodiversity and human welfare. Proceedings of the Indian National Science Academy, 88, 160–171. https://doi.org/10.1007/s43538-022-00073-6
Sillero, N., Arenas-Castro, S., Enriquez‐Urzelai, U., Vale, C. G., Sousa-Guedes, D., Martínez-Freiría, F., Real, R., & Barbosa, A. M. (2021). Want to model a species niche? A step-by-step guideline on correlative ecological niche modelling. Ecological Modelling, 456, 109671. https://doi.org/10.1016/j.ecolmodel.2021.109671
Sinervo, B., Méndez-de la Cruz, F., Miles, D. B., Heulin, B., Bastiaans, E., Cruz, M. V. S., Sites, J. W. Jr. (2010). Erosion of lizard diversity by climate change and altered thermal niches. Science, 328, 894–899. https://doi.org/10.1126/science.1184695
Sinervo, B., Lara-Reséndiz, R. A., Miles, D. B., Lovich, J. E., Rosen, P. C., Gadsden, H., … Méndez de la Cruz, F. (2024). Climate change and collapsing thermal niches of desert reptiles and amphibians: Assisted migration and acclimation rescue from extirpation. Science of the Total Environment, 908, 168431. https://doi.org/10.1016/j.scitotenv.2023.168431
Singh, S. K., Das, D., & Rhen, T. (2020). Embryonic temperature programs phenotype in reptiles. Frontiers in Physiology, 11, 35. https://doi.org/10.3389/fphys.2020.00035
S’khifa, A., Koziel, G., Vences, M., Carretero, M. A., & Slimani, T. (2020). Ecophysiology of a lacertid community in the high Moroccan mountains suggests conservation guidelines. Journal of Thermal Biology, 94, 102743. https://doi.org/10.1016/j.jtherbio.2020.102743
Skulan, J. (2000). Has the importance of the amniote egg been overstated? Zoological Journal of the Linnean Society, 130, 235–261. https://doi.org/10.1006/zjls.1999.0221
Somero, G. N. (2012). The physiology of global change: Linking patterns to mechanisms. Annual Review of Marine Science, 4, 39–61. https://doi.org/10.1146/annurev-marine-120710-100935
Souza-Oliveira, A. F., Zuquim, G., Martins, L. F., Bandeira, L. N., Diele-Viegas, L. M., Cavalcante, V. H. G. L., … Werneck, F. P. (2024). The role of environmental gradients and microclimates in structuring communities and functional groups of lizards in a rainforest–savanna transition area. PeerJ, 12, e16986. https://doi.org/10.7717/peerj.16986
Sunday, J., Bennett, J. M., Calosi, P., Clusella-Trullas, S., Gravel, S., Hargreaves, A. L., … Morales-Castilla, I. (2019). Thermal tolerance patterns across latitude and elevation. Philosophical Transactions of the Royal Society B: Biological Sciences, 374, 20190036. https://doi.org/10.1098/rstb.2019.0036
Taylor, E. N., Diele-Viegas, L. M., Gangloff, E. J., Hall, J. M., Halpern, B., Massey, M. D., … Telemeco, R. S. (2021). The thermal ecology and physiology of reptiles and amphibians: A user’s guide. Journal of Experimental Zoology Part A: Ecological and Integrative Physiology, 335, 13–44. https://doi.org/10.1002/jez.2396
Te Wierik, S. A., Cammeraat, E. L. H., Gupta, J., & Artzy‐Randrup, Y. A. (2021). Reviewing the impact of land use and land‐use change on moisture recycling and precipitation patterns. Water Resources Research, 57, e2020WR029234. https://doi.org/10.1029/2020WR029234
Tewksbury, J. J., Huey, R. B., & Deutsch, C. A. (2008). Putting the heat on tropical animals. Science, 320, 1296–1297. https://doi.org/10.1126/science.1159328
Tracy, C. R., Nussear, K. E., Esque, T. C., Dean-Bradley, K., Tracy, C. R., DeFalco, L. A., Barber, A. M. (2006). The importance of physiological ecology in conservation biology. Integrative and Comparative Biology, 46, 1191–1205. https://doi.org/10.1093/icb/icl054
Tüzün, N., & Stoks, R. (2018). Evolution of geographic variation in thermal performance curves in the face of climate change and implications for biotic interactions. Current Opinion in Insect Science, 29, 78–84. https://doi.org/10.1016/j.cois.2018.07.004
Valenzuela, N., Literman, R., Neuwald, J. L., Mizoguchi, B., Iverson, J. B., Riley, J. L., & Litzgus, J. D. (2019). Extreme thermal fluctuations from climate change unexpectedly accelerate demographic collapse of vertebrates with temperature-dependent sex determination. Scientific Reports, 9, 4254. https://doi.org/10.1038/s41598-019-40597-4
Vardi, R., Dubiner, S., Ben Bezalel, R., Meiri, S., & Levin, E. (2023). Do urban habitats induce physiological changes in Mediterranean lizards? Journal of Zoology, 321, 75–82. https://doi.org/10.1111/jzo.13089
Virens, E., & Cree, A. (2019). Pregnancy reduces critical thermal maximum, but not voluntary thermal maximum, in a viviparous skink. Journal of Comparative Physiology B: Biochemical, Systemic, and Environmental Physiology, 189, 611–621. https://doi.org/10.1007/s00360-019-01230-y
Wang, Y., Li, S.-R., Zeng, Z.-G., Liang, L., & Du, W.-G. (2017). Maternal food availability affects offspring performance and survival in a viviparous lizard. Functional Ecology, 31, 1950–1956. https://doi.org/10.1111/1365-2435.12903
Weaver, S. J., McIntyre, T., Van Rossum, T., Telemeco, R. S., & Taylor, E. N. (2023). Hydration and evaporative water loss of lizards change in response to temperature and humidity acclimation. Journal of Experimental Biology, 226, jeb246459. https://doi.org/10.1242/jeb.246459
Whittington, C. M., Van Dyke, J. U., Liang, S. Q. T., Edwards, S. V., Shine, R., Thompson, M. B., & Grueber, C. E. (2022). Understanding the evolution of viviparity using intraspecific variation in reproductive mode and transitional forms of pregnancy. Biological Reviews, 97, 1179–1192. https://doi.org/10.1111/brv.12836
Wiescher, P. T., Pearce-Duvet, J. M. C., & Feener, D. H. (2012). Assembling an ant community: Species functional traits reflect environmental filtering. Oecologia, 169, 1063–1074. https://doi.org/10.1007/s00442-012-2262-7
Williams, S. E., Shoo, L. P., Isaac, J. L., Hoffmann, A. A., & Langham, G. (2008). Towards an integrated framework for assessing the vulnerability of species to climate change. PLoS Biology, 6, e325. https://doi.org/10.1371/journal.pbio.0060325
Winter, M., Fiedler, W., Hochachka, W. M., Koehncke, A., Meiri, S., & De la Riva, I. (2016). Patterns and biases in climate change research on amphibians and reptiles: A systematic review. Royal Society Open Science, 3, 160158. https://doi.org/10.1098/rsos.160158