ecosistemas
ISSN 1697-2473
Open access / CC BY-NC 4.0
© 2026 Los autores [ECOSISTEMAS no se hace responsable del uso indebido de material sujeto a derecho de autor] / © 2026 The authors [ECOSISTEMAS is not responsible for the misuse of copyrighted material]
Ecosistemas 35(1): 3088 [enero - abril / January - April, 2026]: https://doi.org/10.7818/ECOS.3088
MONOGRÁFICO: Ecología del despoblamiento rural/ MONOGRAPHIC: Ecology of rural depopulation
Editores invitados / Guest editors: Francisco Lloret y Adrián Escudero
ARTÍCULO DE INVESTIGACIÓN / RESEARCH ARTICLE
Efectos del abandono de la ganadería extensiva en la estructura y composición de comunidades de vertebrados necrófagos
Rocío R. Daza1,* ![]() , Pablo Acebes1,2
, Pablo Acebes1,2 ![]() , Juan J. Oñate1,2
, Juan J. Oñate1,2 ![]() , Javier Viñuela3
, Javier Viñuela3 ![]() , Juan Carlos Blanco4
, Juan Carlos Blanco4 ![]() , Pedro P. Olea1,2,*
, Pedro P. Olea1,2,* ![]()
(1) Grupo de Ecología Terrestre (TEG), Departamento de Ecología, Universidad Autónoma de Madrid, Darwin 2, Madrid 28049, España.
(2) Centro de Investigación en Biodiversidad y Cambio Global (CIBC-UAM), Universidad Autónoma de Madrid, Darwin 2, Madrid 28049, España.
(3) Instituto de Investigación en Recursos Cinegéticos (IREC; CSIC-UCLM-JCCM). Ronda de Toledo 55 13071, Ciudad Real, España
(4) Consultores en Biología de la Conservación, Madrid, España.
* A utores para correspondencia / Corresponding authors: Rocío R. Daza [rocio.ruizd@uam.es] Pedro P. Olea [pedrop.olea@uam.es]
|
> Recibido / Received: 26/07/2025 – Aceptado / Accepted: 16/10/2025 |
Cómo citar / How to cite: Daza, R. R., Acebes, P., Oñate, J. J., Viñuela, J., Blanco, J. C., & Olea, P. P. (2026). Efectos del abandono de la ganadería extensiva en la estructura y composición de comunidades de vertebrados necrófagos. Ecosistemas 35(1): 3088. https://doi.org/10.7818/ECOS.3088
|
Efectos del abandono de la ganadería extensiva en la estructura y composición de comunidades de vertebrados necrófagos Resumen: Las comunidades de vertebrados necrófagos desempeñan un papel crucial en el funcionamiento de los ecosistemas al eliminar y reciclar materia animal muerta (carroña). El abandono de la ganadería extensiva, asociado con frecuencia al despoblamiento rural, es responsable de la transformación de numerosos hábitats en grandes extensiones de Europa, especialmente en áreas de montaña, lo que puede alterar las dinámicas ecológicas de estas comunidades. En este estudio experimental evaluamos el impacto del abandono de la ganadería extensiva sobre las comunidades de vertebrados necrófagos en un área de montaña del Sistema Central (España), comparando parcelas con y sin actividad ganadera mediante el uso de pequeñas carroñas (pollos enteros y emplumados, 0.3–1.2 kg) y técnicas de fototrampeo. Asimismo, realizamos una partición de la diversidad a distintas escalas espaciales (alfa, beta y gamma) y evaluamos la influencia del tipo de hábitat y la estructura de la vegetación sobre la diversidad y composición de estas comunidades. La diversidad beta (variación espacial en la composición de especies), contribuyó significativamente a la diversidad regional del área de estudio (gamma), especialmente en hábitats pastoreados, probablemente por la impredecibilidad espacio-temporal del recurso, que favorece procesos estocásticos en el ensamblaje de especies. Los hábitats abandonados albergaron comunidades menos diversas y funcionalmente empobrecidas debido a la pérdida de gremios de necrófagos funcionales claves —como necrófagos obligados (buitres) y depredadores apicales (i.e., águila imperial). Estas comunidades, además, se caracterizaron por su estructura anidada —siendo subconjuntos de las especies presentes en hábitats pastoreados— y estuvieron dominadas por mamíferos mesodepredadores y omnívoros. Finalmente, discutimos el papel de la renaturalización pasiva (passive rewilding) en la consecución de los objetivos de la Ley Europea de Restauración de la Naturaleza, como alternativa a los enfoques tradicionales de gestión activa de tierras agrarias y forestales Palabras clave: carroña; funcionamiento del ecosistema; gestión del territorio; necrófagos facultativos; renaturalización pasiva; sucesión ecológica Effects of extensive livestock abandonment on the structure and composition of vertebrate scavenger assemblages Abstract: Scavenger vertebrate communities play a crucial role in ecosystem functioning through the removal and recycling of dead animal matter (carrion). The abandonment of extensive livestock farming, often associated to rural depopulation, is driving widespread habitat transformation across large areas of Europe, particularly in mountain regions, potentially altering the ecological dynamics of these communities. In this experimental study, we evaluated the impact of extensive livestock abandonment on vertebrate scavenger communities in a mountain area of the Central System (Spain), comparing plots with and without livestock activity using small carcasses (whole feathered chickens, 0.3–1.2 kg) monitored with camera traps. We partitioned diversity across multiple spatial scales (alpha, beta, and gamma) and examined the influence of habitat type and vegetation structure on community diversity and composition. Beta diversity (spatial variation in species composition) contributed significantly to regional diversity (gamma) of the study area, especially in grazed habitats—likely due to the spatio-temporal unpredictability of resources, which favours stochastic species assembly processes. Abandoned habitats hosted less diverse and functionally impoverished communities, driven by the loss of key functional scavenger guilds such as obligate scavengers (vultures) and apex predators (e.g., imperial eagle). These communities were also characterized by a nested structure, comprising subsets of the species found in grazed habitats, and were dominated by mesopredators and omnivorous mammals. Finally, we discuss the role of passive rewilding as a potential strategy to meet the goals of the European Nature Restoration Law, offering an alternative to traditional approaches based on active management of agricultural and forested lands. Keywords: carrion; ecological succession; ecosystem functioning; facultative scavengers; passive rewilding; territory management |
Introducción
Desde el inicio de la agricultura y la ganadería, las actividades humanas han transformado los paisajes mediterráneos, alterando la distribución y abundancia de las especies, así como el funcionamiento de los ecosistemas (Blondel y Aronson, 1999). En estas regiones, la ganadería extensiva tradicional ha sido una de las principales fuerzas modeladoras del paisaje, generando hábitats abiertos y heterogéneos que han favorecido una elevada biodiversidad y la provisión de múltiples servicios ecosistémicos (Fischer et al., 2012; Plieninger et al., 2016). Estos sistemas, considerados como sistemas de Alto Valor Natural (High Nature Value farming systems, HNV; Opperman et al., 2012), son elementos fundamentales para la conservación de la biodiversidad y de los paisajes culturales europeos (Fahrig et al., 2011). Sin embargo, desde mediados del siglo XX, diversos cambios socioeconómicos han provocado una progresiva pérdida de población rural y el abandono de estas prácticas agropecuarias tradicionales, como resultado de la escasa rentabilidad de las explotaciones, especialmente las familiares y las de pequeño tamaño, la falta de relevo generacional y un insuficiente apoyo institucional (MacDonald et al., 2000; Plieninger et al., 2006, 2016; Ustaoglu y Collier, 2018). Se estima que para 2030 hasta el 30 % de la superficie agrícola de la UE-27 —alrededor de 56 millones de hectáreas— está en riesgo de abandono, especialmente en las zonas de montaña (Schuh et al., 2020). La magnitud del fenómeno subraya la urgencia de comprender las consecuencias ecológicas de este proceso.
Una de las consecuencias ecológicas más evidentes del declive y abandono de la ganadería extensiva es la transformación progresiva de los hábitats y paisajes (MacDonald et al., 2000; Pereira y Navarro, 2015; Perino et al., 2019). Tras el cese o reducción de la presión de herbivoría por el ganado y de las actuaciones de aclareo, que con frecuencia realizaban pastores y ganaderos, los pastizales abiertos, dehesas o paisajes agroforestales con escasa o moderada cobertura arbustiva y arbórea, experimentan un proceso de sucesión ecológica secundaria y regeneración espontánea que favorece la expansión del matorral y la regeneración forestal (Pereira y Navarro, 2015; Perino et al., 2019; Frei et al., 2024). Este proceso, conocido también como renaturalización pasiva (passive rewilding), se plantea como una estrategia de restauración ecológica que pretende recuperar la integridad de los ecosistemas con nula o mínima intervención humana (Pereira y Navarro, 2015; Perino et al., 2019; García et al., 2023; Mutillod et al., 2024). Sin embargo, sus efectos sobre la biodiversidad y el funcionamiento de los ecosistemas siguen siendo poco conocidos y, en muchos casos, puramente teóricos (Queiroz et al, 2014; Svenning et al., 2016; Pettorelli et al., 2018; García et al., 2023), especialmente en lo que respecta a grupos funcionales clave en los ecosistemas (p. ej., depredadores apicales, ungulados silvestres, polinizadores o necrófagos).
La descomposición de la materia animal muerta (carroña) es uno de los procesos ecológicos fundamentales en el funcionamiento de los ecosistemas (Cardinale et al., 2012). El consumo de carroña (necrofagia) es una estrategia alimentaria ampliamente extendida entre los vertebrados (Wilson y Wolkovich, 2011), lo que propicia la agregación de una gran diversidad de especies en torno a los cadáveres (Mateo‐Tomás et al., 2015; Olea et al., 2019). Estos ensamblajes están conformados tanto por necrófagos obligados —como los buitres— como facultativos, entre los que se incluyen depredadores apicales, mesodepredadores, rapaces y córvidos, entre otros. Todos ellos contribuyen a la provisión de servicios ecosistémicos esenciales asociados al consumo de carroña, como la regulación del ciclo de nutrientes y la limitación en la propagación de patógenos y enfermedades en el medio natural (Moleón et al., 2014; Olea et al., 2019).
Diversos factores bióticos y abióticos determinan la diversidad y composición de las comunidades de vertebrados necrófagos (p.ej., características del hábitat y de la carroña, temperatura, humedad, interacciones inter- e intraespecíficas; Selva et al., 2005; Moleón et al., 2015; Sebastián-González et al., 2016; Turner et al., 2017; Pardo-Barquín et al., 2019; Cabrera-García et al., 2025). Entre ellos, la configuración y características del hábitat a escala local actúan como un filtro ambiental que influye directamente en la capacidad de las especies para detectar y acceder al recurso (Pardo-Barquín et al., 2019). En consecuencia, el tipo de hábitat modula la composición y estructura de los ensamblajes de necrófagos (Pardo-Barquín et al., 2019; Cabrera-García et al., 2025), así como las dinámicas y la eficiencia del proceso de eliminación de la carroña (Spencer et al., 2024).
En este contexto, el abandono de la ganadería extensiva puede afectar a las comunidades de necrófagos de dos formas: por un lado, reduciendo directamente la disponibilidad de carroñas asociadas a la actividad ganadera (Arrondo et al., 2019), así como la de las presas de los depredadores necrófagos facultativos; por otro, modificando la estructura y composición del hábitat, lo que puede dificultar la localización y el acceso al recurso o alterar las dinámicas de consumo, aunque este aspecto sigue estando poco explorado (pero véanse Arrondo et al., 2019; Martin-Díaz et al., 2020; Oliva-Vidal et al., 2022). En este sentido, Oliva-Vidal et al. (2022) observaron que la regeneración progresiva de la vegetación leñosa tras el abandono de tierras anteriormente con uso ganadero reduce la frecuencia de consumo de los necrófagos obligados, aumentando la persistencia de los cadáveres y favoreciendo el acceso de mamíferos generalistas. A pesar de estos avances, la mayoría de los estudios se han centrado en carroñas de gran tamaño, como las de ungulados domésticos o silvestres, mientras que las carroñas de pequeño tamaño (< 2-3 kg; DeVault y Rhodes, 2002; Turner et al., 2017) han recibido mucha menos atención, si bien presentan mayor frecuencia y biomasa total en los ecosistemas (Barton et al., 2019). Debido al carácter más impredecible y efímero de este tipo de recurso (DeVault et al., 2003; Cortés-Avizanda et al., 2012; Romero, 2020), los necrófagos tienen menos oportunidades para acceder a él, lo que limita la formación de grandes ensamblajes de especies y modifica tanto la estructura de las comunidades como sus dinámicas de consumo comparado con carroñas de mayor tamaño (Moleón et al., 2015).
Para entender los efectos de los cambios de los usos del suelo en la biodiversidad es necesario comprender como ésta se organiza en diferentes contextos ecológicos y a múltiples escalas espaciales, incorporando un enfoque multidimensional y multiescalar. Una aproximación ampliamente utilizada es particionar la biodiversidad en sus componentes alfa, beta y gamma, lo que se ha demostrado útil para entender cómo se estructuran los ensamblajes de especies y las (meta)comunidades en el paisaje (Jost, 2007; Socolar et al., 2016). El objetivo de este trabajo es evaluar el impacto del abandono de la ganadería extensiva sobre la estructura (métricas de diversidad a distintas escalas espaciales) y composición (identidad y abundancia de especies) de las comunidades de vertebrados que consumen carroñas de pequeño tamaño en un área de montaña del Sistema Central (España). Para ello, se empleó un diseño pareado comparando parcelas donde se ha abandonado la actividad ganadera, con parcelas que mantienen el uso ganadero extensivo. Hipotetizamos que el abandono de la ganadería extensiva determina cambios en la estructura y composición de las comunidades de necrófagos. Esto se debe a que el cese del pastoreo favorece la regeneración de la vegetación leñosa de manera espontánea, cuyo resultado más visible es un hábitat estructuralmente más cerrado, alterando las dinámicas de acceso a las carroñas y su consumo por parte de las comunidades de necrófagos (Arrondo et al., 2019; Oliva-Vidal et al., 2022). Además, los procesos de selección de hábitat a diferentes escalas por parte de las especies contribuirán a modificar tanto la composición como la organización funcional de dichas comunidades. Así, predecimos que las parcelas pastoreadas albergarán comunidades con una mayor diversidad y una composición, tanto de especies como de grupos funcionales, diferente a la observada en parcelas abandonadas.
Material y métodos
Área de estudio
El estudio se desarrolló en un ecosistema mediterráneo de la vertiente sur de la Sierra de Guadarrama (Madrid, España), abarcando 1500 km² entre 800 y 1400 m s.n.m (Fig. 1). Las principales coberturas del suelo son pastizales, dehesas, matorrales (principalmente de Cistus ladanifer), encinares (Quercus rotundifolia, acompañado de Juniperus oxycedrus) y bosques de roble melojo (Quercus pyrenaica), excluyéndose del estudio los bosques de pino silvestre (Pinus sylvestris). La región presenta una larga tradición de ganadería extensiva, actualmente en retroceso, con procesos de abandono y renaturalización pasiva que han duplicado la cobertura arbórea y arbustiva en las últimas tres décadas (Acebes et al., 2021). Actualmente, predomina el ganado vacuno, aunque persisten rebaños de ovejas y cabras. La trashumancia, aunque antaño era una práctica común, se ha extinguido en la zona.
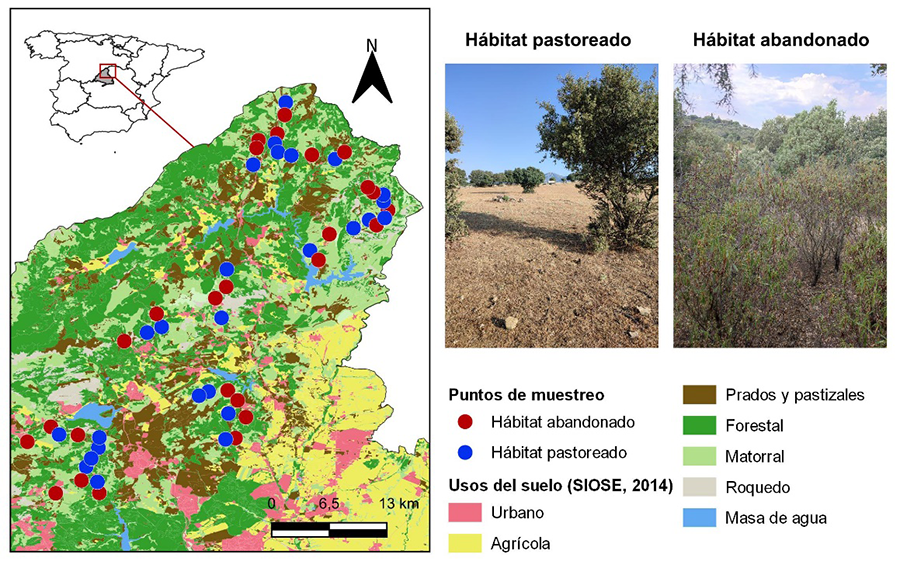
Figura 1. Distribución de los puntos de muestreo correspondientes a hábitats pastoreados (azul) y hábitats abandonados (rojo) en la vertiente sur de la Sierra de Guadarrama (Madrid, España). El mapa base muestra los principales usos del suelo según la base de datos SIOSE 2014. A la derecha, se incluyen imágenes representativas de cada tipo de hábitat.
Figure 1. Distribution of sampling points corresponding to grazed habitats (blue) and abandoned habitats (red) on the southern slope of the Sierra de Guadarrama (Madrid, Spain). The base map shows the main land cover types according to the SIOSE 2014 database. Representative images of each habitat type are shown on the right.
Puntos de muestreo
Se empleó un diseño experimental consistente en un sistema de parcelas pareadas: hábitats actualmente pastoreados (en lo sucesivo denominados «hábitats pastoreados») y hábitats abandonados-renaturalizados (en lo sucesivo denominados «hábitats abandonados»). Las parcelas fueron seleccionadas mediante ortofotos históricas (1956–2020): identificamos áreas que habían sido pastoreadas en el pasado y que, tras su abandono, han experimentado procesos de regeneración de vegetación leñosa, y parcelas que antaño tenían uso ganadero y que seguían siendo pastadas/ramoneadas. Posteriormente, se realizó una validación en el campo de las parcelas seleccionadas para comprobar que, efectivamente, seguían sin y con uso ganadero. Cada pareja de parcelas representaba diferentes etapas de sucesión ecológica de un tipo de hábitat (por ejemplo, pastizales pastoreados de encinas más o menos dispersas frente a encinares más cerrados y matorralizados resultantes del cese de la actividad ganadera). Se establecieron 52 parcelas (26 por tipo de hábitat), de 2x2 km, separadas en promedio 2.6 km (rango: 1.1–6.1 km) para asegurar independencia espacial. En cada parcela se delimitó un área de 10 m de radio en torno a la carroña y la cámara, en los cuales se tomaron medidas de visu de la cobertura arbórea y de matorral, además de su altura (bajo porte, <1 m y alto porte, >1 m). De esta manera, los hábitats pastoreados presentaban una estructura abierta mantenida por la presión de herbivoría del ganado y una baja cobertura de leñosas (cobertura media: 15.5 % de arbolado y 19 % de matorral), aunque no disponemos de información precisa sobre el tipo de ganado, su carga ni la intensidad de pastoreo en cada parcela. Los hábitats abandonados presentaron signos de sucesión secundaria avanzada, con mayor cobertura arbórea (51 %) y de matorral (61 %; véase Figuras A1 y A2 del Anexo para más información).
Monitoreo de carroñas
Durante el verano de 2022 (junio-julio) en cada parcela se instaló una cámara de fototrampeo Browning Dark Ops HD Pro a 2-3 metros apuntando a un único cadáver de pollo, entero y emplumado (300-1.320 g; Tabla A1 del Anexo). Los pollos se pintaron con colorante marrón inocuo y se anclaron al suelo para que no fueran desplazados fuera del campo de visión de la cámara. Las cámaras se programaron para tomar tres imágenes seguidas por activación del sensor de movimiento, con un periodo de inactividad posterior de 1 segundo, y permanecieron activas las 24 horas durante al menos 5 días (normalmente de lunes a viernes, a fin de evitar la alta concurrencia de visitantes los fines de semana y reducir el riesgo de interferencias y sustracción del material). Si la carroña no era consumida en ese periodo, el monitoreo se extendía hasta 7 días; en caso de que la carroña persistiera más tiempo, se prolongaba en intervalos semanales hasta su consumo completo. El tiempo medio de eliminación de las carroñas fue 40.27 ± 28.24 horas en hábitats pastoreados y 104.64 ± 109.30 horas en hábitats abandonados (Daza et al., 2025).
Se registraron todas las especies de vertebrados necrófagos que accedieron a las carroñas, ya fuera para alimentarse o inspeccionarlas, desde su instalación hasta la recogida del material, una vez que la carroña había sido completamente eliminada o solo quedaban huesos y plumas. Se consideró que una especie había consumido carroña cuando las imágenes mostraban evidencia inequívoca de ingesta o, en su defecto, si la especie fue registrada alimentándose al menos una vez en alguna de las 52 parcelas del área de estudio. También se registró la abundancia mínima para cada especie de necrófago por cadáver, utilizando un enfoque conservador. Para ello, de la serie de fotogramas correspondientes a una misma especie en una carroña, seleccionamos aquel fotograma que mostraba el mayor número de individuos presentes de manera simultánea, y asignamos ese valor como abundancia de esa especie en esa carroña. Se registró el número total de individuos presentes, consumieran o no. Luego se corrigió esta abundancia mínima, cuando fue posible, utilizando características morfológicas distintivas (patrones de pelaje, marcas, tamaño corporal, signos de sarna, etc.) para identificar diferentes individuos de la misma especie alimentándose de una misma carroña (véase Mateo‐Tomás et al., 2017 para más detalles).
Análisis de datos
Para evaluar la riqueza de especies y la completitud del muestreo (es decir, la ratio entre el número de especies observadas y la riqueza “verdadera” (Chao y Jost, 2015)), se construyeron curvas de interpolación y extrapolación basadas en la cobertura de la muestra y los números de Hill (Chao et al., 2014; Hsieh et al., 2016). Los números de Hill (Jost, 2006), parametrizados mediante órdenes de diversidad q = 0 (riqueza de especies), q = 1 (diversidad de Shannon) y q = 2 (diversidad de Simpson), se calcularon tanto para la comunidad en general, como por separado para cada tipo de hábitat. Las curvas de acumulación de especies se generaron utilizando la función iNEXT (iNterpolation and EXTrapolation of Hill numbers) del paquete iNEXT (Hsieh et al., 2024) en R (R Core Team, 2025), empleando un enfoque basado en incidencias (es decir, detección/no detección para un conjunto de muestras, mediante el estimador Chao2). Cada detección de una especie en una carroña/cámara/parcela, se contabilizó como una presencia. La incidencia total se obtuvo sumando todas estas presencias de todas las especies en todas las parcelas de muestreo. Se estableció un valor de extrapolación equivalente al doble del número máximo de unidades de muestreo por hábitat (n = 26 × 2 = 52; más allá del doble muestral la estimación no sería fiable: Chao et al., 2014). Los intervalos de confianza para las estimaciones de riqueza y diversidad se calcularon mediante 999 réplicas Bootstrap. Además, para permitir comparaciones más robustas entre hábitats, se estimaron los valores de riqueza y diversidad para un nivel común de completitud muestral (88 %) en base al hábitat con menor cobertura muestral (Tabla A2 de Anexo).
Se realizó una partición de la diversidad desde una aproximación multiplicativa (γ = α × β; Whittaker, 1960), analizándose en tres niveles jerárquicos: 1) carroña (n = 52); 2) hábitat (pastoreado o abandonado); y 3) el área de estudio completa. La diversidad se calculó para cada tipo de hábitat a nivel de carroña (α1) y entre carroñas (β1), dentro (α2) y entre hábitats (β2) y, por último, para el área de estudio completa (γ) (ver Cabrera-García et al., 2025 para una aproximación similar). Las métricas de diversidad se calcularon utilizando la función diversity del paquete vegan (Oksanen et al., 2025) y, posteriormente, los valores de diversidad de Shannon fueron transformados a un número efectivo de especies (números de Hill) para su posterior comparación con los resultados de las curvas de acumulación de especies (Chao et al., 2014). Para comparar la beta multiplicativa entre grupos con distintas unidades muestrales utilizamos la fórmula (qDβ-1)/(N-1) (Jost, 2007), donde Dβ es la β diversidad de orden q y N es el número de unidades muestrales evaluado (Cabrera-García et al., 2025). Este estadístico mide la proporción de diferenciación (o tasa de recambio) entre los conjuntos comparados, variando entre 0 (ninguna diferenciación) y 1 (completa diferenciación). Para determinar si la diversidad mostró un patrón estructural diferente del azar se realizó un análisis de permutación con 9999 permutaciones, para obtener la distribución nula de cada componente de la diversidad.
Posteriormente, se descompuso la diversidad beta para distinguir si las diferencias en la composición de especies entre comunidades se debieron principalmente a un recambio de especies (turnover) o a un patrón de anidamiento (nestedness), donde comunidades más pobres son subconjuntos de comunidades más ricas (Mateo-Tomás et al., 2019). Para ello se calculó la beta diversidad del índice de Jaccard a partir de matrices de presencia/ausencia de las especies con el paquete betapart en R (Baselga et al., 2023).
Para explorar cambios en la composición de las comunidades de vertebrados necrófagos según el tipo de hábitat, se aplicaron dos enfoques diferentes. Primero, para analizar las diferencias en la organización funcional de las comunidades entre hábitats, las 19 especies registradas fueron clasificadas en gremios funcionales, que combinaban características funcionales (grado de especialización en el consumo de carroña: obligado o facultativo), tróficas (posición en la red trófica: depredador apical, mesodepredador u omnívoro) y taxonómicas (distinciones por grupo taxonómico: reptiles, aves y mamíferos). Se compararon las abundancias de los distintos gremios funcionales entre hábitats (pastoreado vs. abandonado) mediante tablas de contingencia (7 grupos × 2 hábitats) con pruebas de chi-cuadrado. En segundo lugar, se realizó un Análisis de Ordenación de Redundancia Basado en Distancias (dbRDA) para explorar los efectos de las características del hábitat sobre la composición de las comunidades de vertebrados necrófagos. El análisis se realizó utilizando la función capscale del paquete vegan (Oksanen et al., 2025), empleando la distancia de Bray-Curtis sobre la matriz de abundancias relativas de especies. Como variables explicativas se usaron el tipo de hábitat (2 niveles: pastoreado y abandonado), la cobertura arbórea (en %), la cobertura de matorral (en %), la altura de matorral alto (> 1 m; en m) y la altura de matorral bajo (< 1 m; en m). Estas métricas fueron estimadas de visu en campo en un radio de 10 metros alrededor de la carroña. Previamente al análisis, todas las variables explicativas fueron estandarizadas (media = 0, desviación estándar = 1).
Resultados
Se registraron 264 individuos pertenecientes a 19 especies de vertebrados (sumando un total de 145 incidencias o presencias) consumiendo activamente o inspeccionando los cadáveres en toda el área de estudio (N = 52 parcelas; Tabla A3 del Anexo). En hábitats abandonados, se detectó aproximadamente el 84.1 % de la riqueza total estimada para este hábitat. Se observaron 13 especies, mientras que la curva de extrapolación para el doble del tamaño muestral estimó una riqueza de 15.5 especies (11.02 – 19.90; 95 % IC), lo que sugiere que entre 2 y 3 especies no habrían sido detectadas en este hábitat. En hábitats pastoreados se observaron 19 especies, un 70.4 % de la riqueza estimada para este hábitat (27 especies; rango: 17.56 – 36.50; 95 % IC), indicando que 11 especies no fueron detectadas (ver Olea et al., 2022 para más detalles). Al aplicar una misma cobertura de muestra del 88 % en ambos hábitats, se obtuvo una mayor riqueza de especies en hábitats pastoreados (17.7 especies) que en abandonados (9.98 especies; Tabla 1). Además, las diversidades de Shannon y Simpson fueron consistentemente mayores en los hábitats pastoreados, tanto en los valores observados como en los estimados, lo que indica que, en estos hábitats, no solo hay más riqueza, sino también más especies comunes y abundantes (Fig. 2; Tabla 1).
Tabla 1. Parámetros numéricos obtenidos de las comunidades de vertebrados necrófagos (basada en datos de incidencia y expresada como número efectivo de especies, es decir, números de Hill) en 52 puntos con carroña en hábitats abandonados y pastoreados de la Sierra de Guadarrama, Madrid. Se muestran los valores observados, así como las estimaciones obtenidas mediante interpolación y extrapolación a partir de la cobertura de la muestra (Cmax = 52 unidades de muestreo) y para una cobertura estandarizada del 88% en ambos hábitats (*).
Table 1. Numerical parameters derived from scavenger vertebrate communities (based on incidence data and expressed as effective number of species, i.e., Hill numbers) at 52 carrion sites located in abandoned and grazed habitats of Sierra de Guadarrama, Madrid. The table shows observed values, as well as estimates obtained through interpolation and extrapolation based on sample coverage (Cmax = 52 sampling units) and standardized to 88% sample coverage across both habitat types (*).
|
|
Pastoreado |
Abandonado |
|
Riqueza de especies observada |
19 |
13 |
|
Riqueza de especies estimada (N = 52 (Cmax), IC = 95 %) |
27 (17.56 – 36.50) |
15.46 (11.02 – 19.90) |
|
% de riqueza de especies detectada |
70 % |
84 % |
|
Riqueza de especies estimada (SC= 88 %, IC = 95 %) * |
17.70 (0 – 45.07) |
9.98 (6.94 – 13.02) |
|
Diversidad de Shannon observada |
11.23 |
7.92 |
|
Diversidad de Shannon estimada (N = 52 (Cmax), IC = 95 %) |
12,72 (9.84 – 15.61) |
8.52 (6.46 – 10.58) |
|
Diversidad de Shannon estimada (SC= 88 %, IC = 95 %) * |
10,93 (4.69 – 17.17) |
7.06 (5.68 – 8.43) |
|
Diversidad de Simpson observada |
7.24 |
5.82 |
|
Diversidad de Simpson estimada (N = 52 (Cmax), IC = 95 %) |
7.45 (5.96 – 8.95) |
5.97 (4.43 – 7.51) |
|
Diversidad de Simpson estimada (SC= 88 %, IC = 95 %) * |
7.17 (5.16 – 9.19) |
5.51 (4.56 – 6.47) |
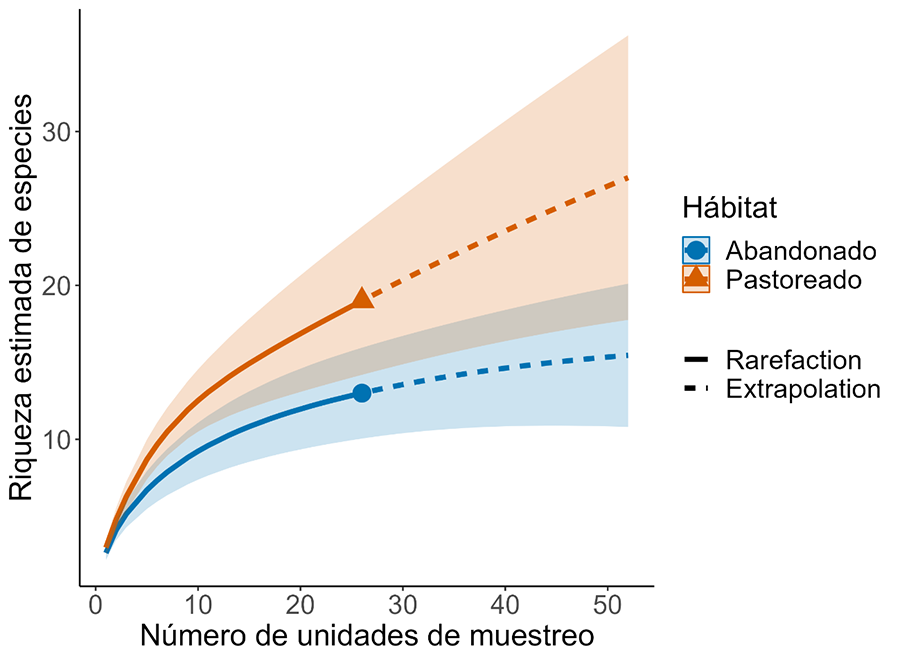
Figura 2. Curvas de acumulación de especies basadas en el tamaño de muestra. Las líneas continuas representan el número observado de especies (números de Hill, q = 0) mediante interpolación, mientras que las líneas discontinuas muestran el número extrapolado de especies hasta el doble del tamaño muestral por tipo de hábitat (N=52), utilizando un enfoque basado en incidencias (estimador Chao2). Las curvas se muestran para dos tipos de hábitat: abandonado (línea azul) y pastoreado (línea naranja). Las áreas sombreadas representan los intervalos de confianza del 95 %.
Figure 2. Sample-size-based species accumulation curves. Solid lines represent the observed number of species (Hill numbers, q = 0) obtained through interpolation, while dashed lines indicate extrapolated species richness up to twice the sample size per habitat type (N = 52), using an incidence-based approach (Chao2 estimator). Curves are shown for two habitat types: abandoned (blue line) and grazed (orange line). Shaded areas represent 95% confidence intervals.
Partición de la diversidad de las comunidades de vertebrados necrófagos
La partición jerárquica de la diversidad mostró que la diversidad de vertebrados necrófagos se distribuyó aleatoriamente entre las distintas escalas espaciales, con algunas excepciones significativas (Tabla 2). Los hábitats pastoreados concentraron toda la riqueza regional observada (diversidad gamma: 19 especies), mientras que los hábitats abandonados albergaron el 68 % de esa riqueza (13 de 19). A nivel de carroña (α₁), la riqueza fue ligeramente superior en los hábitats pastoreados (2.96) respecto a los abandonados (2.61), aunque en ambos casos los valores coincidieron con lo esperado por azar (p > 0.05). Lo mismo ocurrió con la diversidad de Shannon a esta escala. A escala de hábitat (α₂), la riqueza fue significativamente mayor que la esperada por azar en los hábitats pastoreados (19 especies observadas vs. 16.21 esperadas; p < 0.05), pero no en los abandonados (p > 0.05). Un patrón similar se observó para la diversidad de Shannon.
La diversidad beta entre puntos de carroña dentro de cada hábitat (β₁) también fue mayor en hábitats pastoreados que en abandonados, tanto para la riqueza (0.22 vs. 0.15) como para la diversidad de Shannon (0.55 vs. 0.31). En el caso de la riqueza, esta diferencia fue marginalmente significativa (p = 0.08), mientras que para Shannon no se observaron diferencias respecto a una distribución aleatoria (p > 0.05). La diversidad beta entre hábitats (β₂) no se diferenció de la esperado por azar en cuanto a la riqueza (β₂ = 0.19; p > 0.05), pero sí lo hizo para la diversidad de Shannon (p < 0.001), lo que indica una diferenciación significativa en la composición relativa de especies abundantes entre hábitats más allá de lo esperado por azar (Tabla 2).
La disimilitud entre las comunidades de vertebrados necrófagos en ambos tipos de hábitat, medida con el índice de Jaccard, fue del 31.6 %. Esta diferencia se debió exclusivamente al componente de anidamiento (nestedness), ya que todas las especies presentes en el hábitat abandonado (más pobre en especies) también estaban presentes en el hábitat pastoreado. Dentro de cada hábitat, la disimilitud entre unidades de muestreo (carroñas) fue elevada: 71.8 % en pastoreado y 67.2 % en abandonado. En ambos casos, la mayor parte de esta disimilitud se explicó por el reemplazo de especies (turnover): 63.5 % en pastoreado y 78.9 % en abandonado, mientras que el resto se debió al anidamiento (36.5 % y 21.1 %, respectivamente).
Tabla 2. Partición multiplicativa de la riqueza y diversidad de necrófagos (expresada como número efectivo de especies, es decir, números de Hill) en 52 carroñas en hábitats abandonados y pastoreados de la Sierra de Guadarrama, Madrid. La diversidad se particionó jerárquicamente en: (i) diversidad en cada carroña (α₁) y entre carroñas dentro de cada hábitat (β₁), (ii) diversidad por hábitat (α₂) y entre hábitats (β₂), y (iii) diversidad regional (γ del área de estudio). Las métricas beta están estandarizadas (ver Metodología). Los p-valores se obtuvieron a partir de 9999 permutaciones para generar distribuciones nulas de cada componente de diversidad en cada nivel jerárquico. Los valores significativos están en negrita (p < 0.05).
Table 2. Multiplicative partitioning of scavenger species richness and diversity (expressed as effective number of species, i.e., Hill numbers) across 52 carrion sites in abandoned and grazed habitats of the Sierra de Guadarrama, Madrid. Diversity was hierarchically partitioned into: (i) within-carrion diversity (α₁) and among-carrion diversity within each habitat (β₁), (ii) within-habitat diversity (α₂) and among-habitat diversity (β₂), and (iii) regional diversity (γ across the study area). Beta diversity metrics are standardized (see Methods). P-values were obtained from 9999 permutations to generate null distributions for each diversity component at each hierarchical level. Statistically significant values are shown in bold (p < 0.05).
Métrica de diversidad |
Valor observado |
Valor esperado |
p-valor |
|
Riqueza de especies |
|||
|
α1-abandonado |
2.61 |
2.79 |
0.82 |
|
β1-abandonado |
0.15 |
0.19 |
0.97 |
|
α2-abandonado |
13 |
16.17 |
0.99 |
|
α1-pastoreado |
2.96 |
2.79 |
0.23 |
|
β1-pastoreado |
0.22 |
0.19 |
0.08 |
|
α2-pastoreado |
19 |
16.21 |
< 0.05 |
|
β2-entre hábitats |
0.19 |
0.18 |
0.52 |
|
γ (área de estudio) |
19 |
|
|
|
Diversidad de Shannon |
|||
|
α1-abandonado |
2.20 |
2.29 |
0.72 |
|
β1-abandonado |
0.31 |
0.48 |
0.997 |
|
α2-abandonado |
5.48 |
8.23 |
0.998 |
|
α1-pastoreado |
2.38 |
2.29 |
0.28 |
|
β1-pastoreado |
0.55 |
0.48 |
0.19 |
|
α2-pastoreado |
10.39 |
8.26 |
< 0.05 |
|
Jβ2-entre hábitats |
0.15 |
0.06 |
< 0.001 |
|
γ (área de estudio) |
8.71 |
|
|
Composición de la comunidad de vertebrados necrófagos
De las 19 especies que conformaron la comunidad, 11 fueron aves, 7 mamíferos y 1 reptil. Solo una de ellas fue un necrófago obligado, el buitre negro Aegypius monachus, mientras que el resto fueron necrófagos facultativos. A nivel de hábitat, seis especies fueron exclusivas de los hábitats pastoreados, incluyendo el buitre negro, el azor común Accipiter gentilis, el águila imperial Aquila adalberti, el milano negro Milvus migrans, el cuervo Corvus corax y la urraca Pica pica. En contraste, no se detectaron especies exclusivas en los hábitats abandonados (Fig. 3; Tabla A3 del Anexo).
En cuanto a la abundancia relativa de necrófagos en las carroñas, se observaron diferencias entre hábitats para algunas especies. El jabalí Sus scrofa y la garduña Martes foina fueron más abundantes en carroñas de hábitats abandonados, mientras que la corneja Corvus corone fue más abundante en hábitats pastoreados. Por el contrario, el zorro Vulpes vulpes presentó una abundancia similar en ambos tipos de hábitat y fue la especie más abundante en el área de estudio (Fig. 3; Tabla A3 del Anexo).
Se detectaron diferencias significativas en la composición de gremios funcionales entre hábitats (χ² = 53.61; p < 0.001) (Fig. 4). En los hábitats abandonados, la comunidad estuvo dominada por necrófagos facultativos, especialmente por mamíferos omnívoros (49 %) y mesodepredadores carnívoros (39 %), mientras que otros gremios estuvieron escasamente representados (p.ej., rapaces y córvidos) o ausentes (necrófagos obligados y depredadores apicales). En cambio, los hábitats pastoreados mostraron una mayor diversidad funcional. Aunque los mesodepredadores carnívoros facultativos fueron el gremio predominante (41 %), se registraron proporciones más equilibradas entre córvidos (27 %), rapaces (13 %) y mamíferos omnívoros (14 %). Además, en estos hábitats se detectaron necrófagos obligados (buitre negro) y depredadores apicales (águila imperial), no detectados en los hábitats abandonados (Fig. 4).
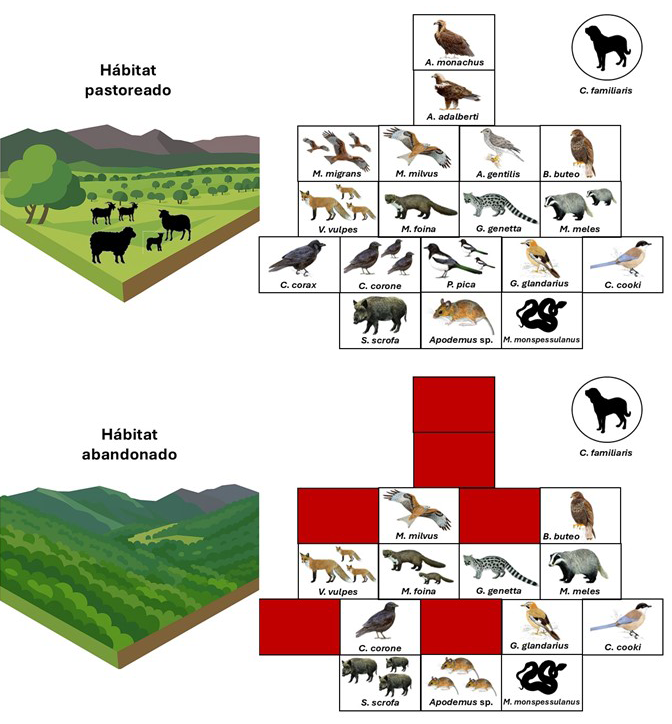
Figura 3. Esquema ilustrativo de los cambios observados en la composición de especies de vertebrados necrófagos en hábitats ganaderos sufriendo procesos de abandono: ejemplo de un paisaje pastoreado (arriba) y abandonado (abajo). Cada recuadro representa una especie, con su abundancia relativa indicada por el número de iconos. Los cuadros rojos indican la ausencia de la especie en ese hábitat. El perro (C. familiaris) se representa por separado, al tratarse de un animal doméstico. Las especies están organizadas siguiendo un gradiente taxonómico-trófico-funcional, desde el necrófago obligado en la cima (buitre negro), hasta los necrófagos facultativos en la base. Estos últimos se agrupan jerárquicamente de arriba a abajo en las siguientes categorías: depredadores apicales, mesodepredadores rapaces, mesodepredadores carnívoros, omnívoros córvidos, omnívoros mamíferos y reptiles. Los iconos de los hábitats fueron generados con ChatGPT. Los iconos de aves provienen de SEO/BirdLife, los de mamíferos de la SECEM, y los del reptil y el perro de la plataforma PhyloPic.
Figure 3. Illustrative scheme of observed changes in the species composition of scavenger vertebrates in livestock-dominated habitats undergoing abandonment processes: example of a grazed landscape (top) and an abandoned one (bottom). Each box represents a species, with its relative abundance indicated by the number of symbols. Red boxes indicate the absence of the species in that habitat. The dog (C. familiaris) is shown separately, as it is a domestic animal. Species are arranged along a taxonomic–trophic–functional gradient, from the obligate scavenger at the top (black vulture), to facultative scavengers at the bottom. These are hierarchically grouped from top to bottom into the following categories: apex predators, raptorial mesopredators, carnivorous mesopredators, corvid omnivores, mammalian omnivores, and reptiles. Habitat icons were generated with ChatGPT. Bird icons are from SEO/BirdLife, mammal icons from SECEM, and reptile and dog icons from the PhyloPic platform.
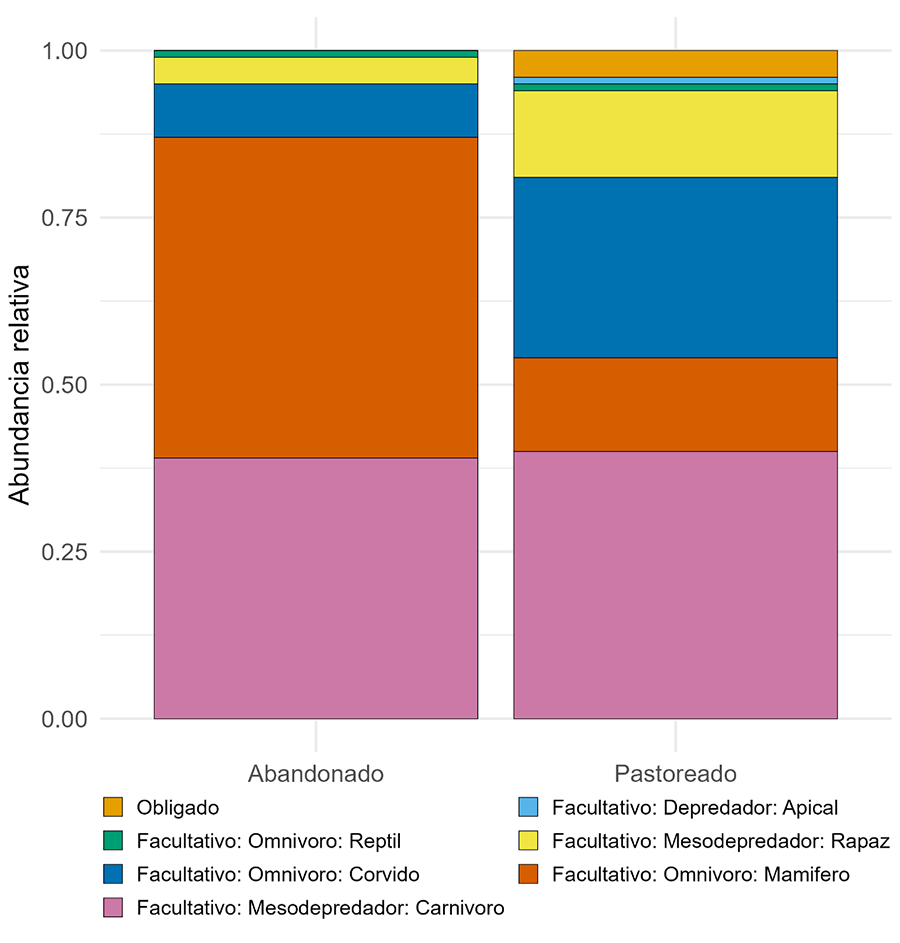
Figura 4. Abundancias relativas de los distintos gremios funcionales de vertebrados necrófagos en hábitats pastoreados y abandonados, definidos de acuerdo con una combinación de características tróficas, funcionales y taxonómicas.
Figure 4. Relative abundance of different functional guilds of scavenger vertebrates in grazed and abandoned habitats, defined by a combination of trophic, functional, and taxonomic characteristics.
El modelo db-RDA fue significativo (F = 2.10; p < 0.001), explicando un 18.8% de la variabilidad total en la composición de especies. Los dos primeros ejes explicaron en conjunto el 70 % de esta variabilidad explicada (R2 CAP1 = 44.6 % y R2 CAP2 = 25.4 %), aunque solo el primer eje (CAP1) fue estadísticamente significativo (p < 0.01). Este eje se correlacionó significativamente con la variable de cobertura arbórea, y separó las parcelas de hábitats abandonados de las pastoreadas (Fig. 5). No obstante, algunos hábitats pastoreados muestreados fueron dehesas, que mantienen una cobertura de arbolado dispersa, situándose en posiciones intermedias a lo largo del eje 1. El segundo eje (CAP2) está asociado principalmente con la cobertura y la altura del matorral. Este eje diferencia las parcelas con abundante presencia de matorral —tanto de matorral bajo (< 1 metro) como alto (> 1 metro)— de aquellas parcelas que presentan un hábitat abierto, carentes de masa arbustiva. El tipo de hábitat fue una variable significativa (r² = 0.15; p < 0.001), indicando diferencias en la composición de la comunidad entre hábitats pastoreados y abandonados (Fig. 5).
Respecto a la asociación de las especies con los ejes del db-RDA y las variables de estructura de la vegetación, la garduña se asoció con parcelas de hábitats abandonados caracterizadas por presentar alta cobertura arbórea y de matorral (relación positiva con CAP1 y negativa con CAP2). El zorro mostró afinidad por lugares con hábitats pastoreados abiertos con escasa cobertura arbórea (relación negativa con CAP1), mientras que el jabalí se vinculó con hábitats abandonados muy forestados (CAP1 positivo). Las rapaces (buitre negro, águila imperial, milano negro y real) y los córvidos (excepto el arrendajo), se asociaron con lugares pastoreados caracterizadas por presentar poca cobertura de matorral (CAP2 positivo) (Fig. 5).
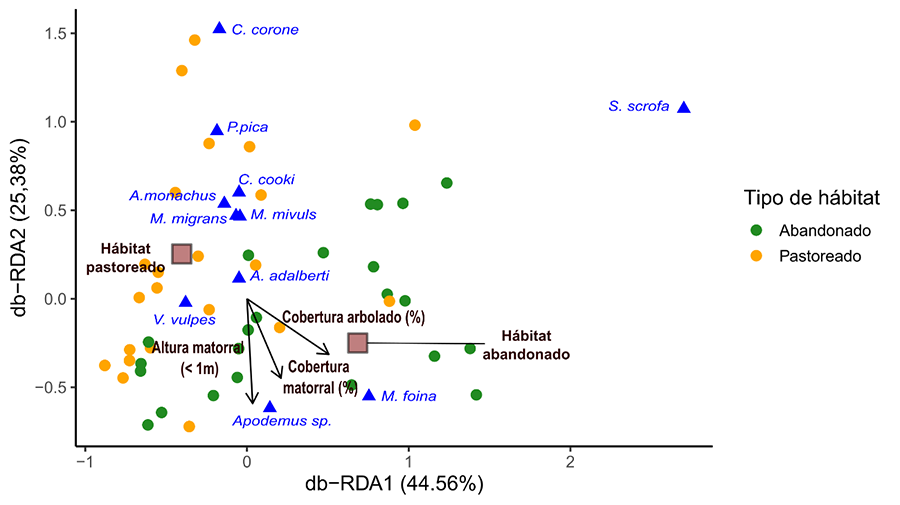
Figura 5. Análisis de Ordenación de Redundancia Basado en Distancias (dbRDA) para explorar los efectos de las características del hábitat sobre la composición de las comunidades de vertebrados necrófagos. Se muestran exclusivamente las variables ambientales significativas (p < 0.05) mediante flechas y las especies asociadas significativamente a alguno de los dos ejes principales del análisis (p < 0.05; triángulos azules). Los cuadrados rojos representan el centroide del tipo de hábitat tratado como un factor.
Figure 5. Distance-based Redundancy Analysis (dbRDA) exploring the effects of habitat characteristics on the composition of scavenger vertebrate communities. Only significant environmental variables (p < 0.05) are shown as arrows, along with species significantly associated with either of the two main ordination axes (p < 0.05; blue triangles). Red squares represent the centroid of each habitat type treated as a categorical factor.
Discusión
En este estudio analizamos cómo el abandono de la ganadería extensiva —un proceso creciente en muchas regiones rurales de Europa (Ustaoglu y Collier, 2018; Fayet et al., 2022) y que conlleva profundas transformaciones en los hábitats— afecta a su vez a la estructura y composición de las comunidades de vertebrados necrófagos en un paisaje mediterráneo de montaña. Nuestros resultados muestran que el abandono de la ganadería extensiva y la consecuente transformación del hábitat alteran significativamente la riqueza y diversidad de las comunidades de vertebrados necrófagos. Además, mostramos que la estructura del hábitat a escala local opera como un filtro ambiental determinante en el ensamblaje y composición de estas comunidades.
Los hábitats pastoreados albergaron mayor diversidad de especies que los hábitats abandonados, tanto en términos de riqueza específica como de diversidad de Shannon, especialmente a escalas espaciales más amplias (α₂). De hecho, los hábitats pastoreados concentraron la totalidad de la riqueza regional observada (19 especies), mientras que los hábitats abandonados representaron únicamente un subconjunto empobrecido de esta comunidad, albergando solo el 68 % de las especies regionales y mostrando mayores dominancias en las frecuencias de aparición. Esta pérdida, más que recambio, de especies observada tras el abandono quedó reflejada por la beta diversidad (β2), que mostró un 31 % de diferenciación entre comunidades atribuible en su totalidad al anidamiento, esto es, a especies compartidas entre ambos tipos de hábitats. La mayor riqueza de especies de los hábitats pastoreados (α2) se explica por la mayor diversidad beta entre carroñas (β1), la cual estuvo dominada por el recambio de especies (63.5 %), indicando una alta variabilidad en la composición de especies entre carroñas. Este recambio de especies probablemente se debe a procesos estocásticos, como el orden de llegada o la detección del recurso, asociados a la alta impredecibilidad de este tipo de carroñas de pequeño tamaño y a procesos determinísticos, como una mayor heterogeneidad ambiental local en estos entornos (DeVault et al., 2003; Cortés-Avizanda et al., 2012; Romero, 2020). Estos resultados destacan la importancia del componente beta de la diversidad y los mecanismos ecológicos que la generan como elementos clave para comprender la organización de las comunidades de necrófagos (Cabrera-García et al., 2025), especialmente en hábitats sometidos a procesos de abandono.
El patrón de diversidad observado sugiere que el abandono de la ganadería extensiva y la transformación del hábitat conllevan una homogeneización biótica, es decir, una pérdida progresiva de especies presentes en los hábitats pastoreados, sin que estas sean reemplazadas por nuevas especies, lo que deriva en una simplificación taxonómica y funcional. En los hábitats abandonados, no se detectaron gremios funcionales clave, como las aves necrófagas obligadas (p.ej., buitre negro) y los depredadores apicales (p.ej., águila imperial), así como varias especies en los gremios de rapaces de tamaño medio y córvidos (Fig. 3 y 4). La pérdida de estas especies, altamente eficientes en la localización y consumo rápido de cadáveres (Ruxton y Houston, 2004), puede tener implicaciones directas sobre el funcionamiento del ecosistema, prolongando la persistencia de los cadáveres en el medio, lo que puede favorecer la proliferación de patógenos y el riesgo de transmisión de enfermedades (Ogada et al., 2012; Morales-Reyes et al., 2017; Daza et al., 2025).
Además, entre las especies que persisten en ambos tipos de hábitat —es decir, aquellas que conforman el componente de anidamiento— se observan variaciones en su abundancia relativa, lo que también contribuye a las diferencias observadas en la estructura y composición de las comunidades. Nuestros resultados muestran que el abandono de la ganadería extensiva beneficia a mamíferos mesodepredadores como la garduña, a omnívoros como el jabalí y a pequeños roedores (Apodemus spp.), que se vuelven más abundantes en hábitats abandonados (Torre et al., 2007). Por el contrario, especies dominantes en hábitats pastoreados como córvidos (p.ej., la corneja) y rapaces como el milano real Milvus milvus, disminuyen notablemente en abundancia conforme aumenta la cobertura arbórea y de matorral (Mougeot et al., 2009). Este patrón coincide con lo observado en otros estudios, donde los paisajes abiertos tienden a sostener comunidades más diversas, con necrófagos obligados y facultativos, mientras que los paisajes cerrados favorecen a especies facultativas y generalistas, como el jabalí, sobre todo si son objeto de alta presión cinegética (Selva et al., 2005; Pardo-Barquín et al., 2019; Arrondo et al., 2019; Oliva-Vidal et al., 2022). Esto puede deberse a que los hábitats abandonados, caracterizados por presentar vegetación más densa y cerrada, dificultan la visibilidad y el acceso al recurso por parte de especies que dependen de la visión para detectar las carroñas y que se desplazan volando, como es el caso de muchas aves necrófagas obligadas, rapaces y córvidos (Ruxton y Houston, 2004; Pardo-Barquín et al., 2019). Por el contrario, estos entornos más cerrados favorecen a la mayoría de los mamíferos, tanto mesodepredadores como omnívoros, que dependen de señales olfativas para localizar los cadáveres y suelen ser activos durante la noche o el crepúsculo (Enari y Enari, 2021). Así, la estructura de la vegetación actúa como un filtro ambiental que no solo condiciona la diversidad local (alfa) y la composición de especies entre hábitats (beta), sino que también podría influir en la eficiencia del proceso de eliminación de carroñas, al condicionar qué especies acceden al recurso y con qué rapidez lo hacen, como se ha observado con carroñas grandes (Spencer et al., 2024).
Además, el propio tamaño de las carroñas utilizadas en este estudio también condicionó los patrones observados de diversidad. Las carroñas pequeñas, por su baja biomasa y alta impredecibilidad, tienden a atraer a un número reducido de especies por evento (Moleón et al., 2015; Oh et al., 2024), lo que se traduce en la baja diversidad alfa observada en ambos tipos de hábitat. Sin embargo, su aparición aleatoria en el tiempo y el espacio genera dinámicas fuertemente estocásticas, donde factores como el orden de llegada o la detección inicial del recurso pueden determinar los patrones sucesionales y el ensamblaje de especies. Esta aleatoriedad reduce la dominancia de especies especializadas y podría haber favorecido una alta variabilidad en la composición de especies entre eventos, lo que se reflejó en una elevada diversidad beta entre carroñas (β₁), especialmente en hábitats pastoreados.
A pesar de la presencia de algunas especies muy comunes como el zorro, el jabalí y el ratón, muchas otras, especialmente aquellas exclusivas de hábitats pastoreados se detectaron de forma ocasional y con baja abundancia relativa. Como resultado, las curvas de extrapolación no alcanzaron la asíntota, lo que sugiere la existencia de un número considerable de especies raras o poco frecuentes que no fueron detectadas. De hecho, las estimaciones indicaron que hasta un 30 % de la riqueza esperada en hábitats pastoreados no fue registrada, debido a especies muy poco frecuentes o raras no observadas, ya que las más comunes fueron detectadas casi completamente (con coberturas de muestreo superiores al 99.7%; Tabla A2 y Fig. A3 del Anexo). Estas especies comunes, con alta conectividad en las carroñas, desempeñan un papel clave en la estructuración de la red trófica y la estabilidad de los ensamblajes de necrófagos (Sebastián-González et al., 2021).
Cabe destacar que, a pesar de haberse utilizado carroñas de pequeño tamaño, se registraron 19 especies, una riqueza considerablemente alta en comparación con otros trabajos similares. Si bien algunos estudios con un esfuerzo de muestreo mucho mayor, como el de Olea et al. (2022), registraron hasta 29 especies en carroñas de pollo, otros trabajos han reportado entre 4 y 13 especies (Turner et al., 2017; Sebastián-González et al., 2013). Incluso es equiparable con estudios que utilizan o comparan diferentes tamaños de carroña, que han registrado entre 10 y 29 especies en carroñas de ungulados domésticos y silvestres (véase Mateo-Tomás et al., 2015; Oliva-Vidal et al., 2022; Cabrera-García et al., 2025). Estos resultados sugieren que, especialmente en hábitats que mantienen la actividad ganadera en extensivo, las carroñas pequeñas pueden sostener comunidades necrófagas altamente diversas a una escala de paisaje.
Este estudio presenta algunas limitaciones que deben ser consideradas al interpretar los resultados. En primer lugar, el muestreo se llevó a cabo exclusivamente durante el verano, lo que podría haber condicionado la estructura y composición observadas de las comunidades de vertebrados necrófagos (DeVault et al., 2004; Turner et al., 2017; Spencer et al., 2024). Por tanto, es posible que algunas especies propias de otras estaciones no hayan sido detectadas, lo que podría haber llevado a una subestimación de la riqueza total de la comunidad de necrófagos. En segundo lugar, el estudio se centró exclusivamente en carroñas de pequeño tamaño, lo cual puede limitar la detección de especies especializadas, como los necrófagos obligados o depredadores apicales, que suelen explotar preferentemente carroñas de mayor biomasa (Ruxton y Houston, 2004). Además, el tamaño muestral es importante en comunidades de necrófagos, donde muchas especies son facultativas y presentan bajas tasas de detección. En estos casos, los estimadores de riqueza pueden verse influidos por la presencia de especies con muy baja incidencia, lo que tiende a sobreestimar los valores en la extrapolación. Por ello, en futuros trabajos se recomienda aumentar el esfuerzo de muestreo, tanto en número de réplicas como en cobertura temporal, para obtener una representación más completa de las comunidades de necrófagos. Asimismo, en hábitats con mayor cobertura de matorral, el campo de visión de la cámara puede ser menor, lo que podría reducir la detectabilidad de ciertos individuos o especies; aunque el uso de la carroña como cebo pudo mitigar en gran medida este efecto. Finalmente, cabe destacar que en cada tipo de hábitat existe una considerable heterogeneidad en la estructura y complejidad de la vegetación a escala local, por lo que futuros estudios deberían centrarse en caracterizarla con mayor detalle para poder controlar su efecto potencial en la detectabilidad de necrófagos.
Aunque la renaturalización ha sido propuesta como vía para cumplir los objetivos de la Ley de Restauración de la Naturaleza (UE, 2024/1991), nuestros resultados sugieren que, en el contexto estudiado, la renaturalización pasiva tras el abandono ganadero puede conllevar efectos contrarios. La reducción de hábitats abiertos mantenidos por el pastoreo implica la pérdida de especies necrófagas (varias protegidas por la Directiva Aves), sin sustitución funcional, lo que simplifica la comunidad biológica. Además, aunque no ha sido cuantificado, es previsible que el avance del matorral y arbolado se produzca a expensas de formaciones herbosas naturales y seminaturales, incluidas en el hábitat prioritario 6220 de la Directiva Hábitats. A corto plazo, predomina la expansión de jarales (Cistus ladanifer) en la zona de estudio, sin que prosperen hábitats leñosos de mayor valor incluidos en la Directiva (aunque no prioritarios como 5210, 4030, 9340, 9380, 91B0 y 9230). Por tanto, alcanzar los objetivos de restauración requeriría combinar medidas de renaturalización activa que promuevan la expansión de formaciones valiosas, con la conservación de comunidades herbáceas protegidas y la creación de paisajes en mosaico. En este marco, las medidas agroambientales de la PAC podrían desempeñar un papel clave (Oñate et al., 2023).
Conclusiones
El abandono de la ganadería extensiva y la consecuente transformación del hábitat provocan una homogeneización taxonómica y funcional de las comunidades de vertebrados necrófagos: pérdida significativa de riqueza y diversidad, con comunidades funcionalmente más simples y dominadas por especies facultativas, especialmente mamíferos mesodepredadores y omnívoros, lo que puede ralentizar procesos ecológicos clave como la eliminación de carroñas. Las carroñas pequeñas sostienen una alta diversidad de necrófagos en los ecosistemas, un patrón que podría explicarse por la alta impredecibilidad espaciotemporal asociada a este tipo de recursos pulsados, que favorece procesos estocásticos en el ensamblaje de especies. A la vista de nuestros resultados, el papel de la renaturalización pasiva para conseguir los objetivos de la Ley de Restauración de la Naturaleza parece cuestionable si no se acompaña de medidas activas que promuevan el mantenimiento de los sistemas agrarios de alto valor natural en la zona.
Contribución de los autores
Rocío R. Daza: Conceptualización, Análisis de datos, Borrador original, Revisión y Edición. Pablo Acebes: Metodología, Trabajo de campo, Obtención de financiación, Revisión y Edición. Juan J. Oñate, Juan Carlos Blanco y Javier Viñuela: Revisión y Edición. Pedro P. Olea: Conceptualización, Metodología, Trabajo de campo, Diseño y supervisión del análisis de datos, Obtención de financiación, Borrador original, Revisión y Edición.
Disponibilidad de datos y código
El código y los datos utilizados en este trabajo se encuentran disponibles en acceso abierto en el repositorio ZENODO: https://doi.org/10.5281/zenodo.18185654.
Financiación / permisos requeridos / potenciales conflictos de interés y/o agradecimientos
Esta investigación fue financiada parcialmente por el proyecto 'Procesos de resilvestrización en ecosistemas mediterráneos' (FUAM: 820052) y por el Ministerio de Ciencia e Innovación, proyecto 'Desafíos y oportunidades para la provisión de funciones y servicios de los ecosistemas en paisajes agrícolas y renaturalizados' (REWILDTEST) (PID2022-142096OB-I00), cofinanciado por el Fondo Europeo de Desarrollo Regional (FEDER, UE). Agradecemos a la Consejería de Medio Ambiente, Ordenación del Territorio y Sostenibilidad y a la Consejería de Medio Ambiente, Agricultura e Interior (Comunidad de Madrid) por concedernos los permisos necesarios para realizar el trabajo de campo en el Parque Nacional de la Sierra de Guadarrama.
Los autores/as declaran no tener ningún conflicto de intereses.
Agradecemos a Iván Herranz por su ayuda durante el trabajo de campo y el procesamiento de datos.
Referencias
Acebes, P., Iglesias-González, Z., & Muñoz-Gálvez, F. J. (2021). Do traditional livestock systems fit into contemporary landscapes? Integrating social perceptions and values on landscape change. Agriculture, 11(11), 1107. https://www.mdpi.com/2077-0472/11/11/1107
Arrondo, E., Morales-Reyes, Z., Moleón, M., Cortés-Avizanda, A., Donázar, J. A., & Sánchez-Zapata, J. A. (2019). Rewilding traditional grazing areas affects scavenger assemblages and carcass consumption patterns. Basic and Applied Ecology, 41, 56–66. https://doi.org/10.1016/j.baae.2019.10.006
Barton, P. S., Evans, M. J., Foster, C. N., Pechal, J. L., Bump, J. K., Quattiotto, M, -M., & Benbow, M. E. (2019). Towards quantifying carrion biomass in ecosystems. Trends in Ecology & Evolution, 34(10), 950–961. https://doi.org/10.1016/j.tree.2019.06.001
Baselga, A., Orme, D., Villeger, S., De Bortoli, J., Leprieur, F., Maxime Logez, … Henriques-Silva, R. (2023). betapart: Partitioning beta diversity into turnover and nestedness components (Version 1.6) [R package]. Retrieved July 2025 from https://cran.r-project.org/package=betapart
Blondel, J., & Aronson, J. (1999). Biology and wildlife of the Mediterranean region. Oxford University Press.
Cabrera-García, M. E., Mateo-Tomás, P., Sarasola, J. H., Zanón Martínez, J. I., Martínez-Miranzo, B., & Olea, P. P. (2025). Unravelling the multi-scale structure of vertebrate scavenger communities: The role of beta-diversity in livestock carcass consumption. Basic and Applied Ecology, 83, 64–72. https://doi.org/10.1016/j.baae.2025.01.008
Cardinale, B., Duffy, J., Gonzalez, A., Hooper, D. U., Perrings, C., Venail, P., … Naeem, S. (2012). Biodiversity loss and its impact on humanity. Nature, 486, 59–67. https://doi.org/10.1038/nature11148
Chao, A., Gotelli, N. J., Hsieh, T. C., Sander, E. L., Ma, K. H., Colwell, R. K., & Ellison, A. M. (2014). Rarefaction and extrapolation with Hill numbers: A framework for sampling and estimation in species diversity studies. Ecological Monographs, 84(1), 45–67. https://doi.org/10.1890/13-0133.1
Chao, A., & Jost, L. (2015). Estimating diversity and entropy profiles via discovery rates of new species. Methods in Ecology and Evolution, 6(8), 873–882. https://doi.org/10.1111/2041-210X.12349
Cortés-Avizanda, A., Jovani, R., Carrete, M., & Donázar, J. A. (2012). Resource unpredictability promotes species diversity and coexistence in an avian scavenger guild: A field experiment. Ecology, 93(12), 2570–2579. https://doi.org/10.1890/12-0221.1
Daza, R. R., Acebes, P., & Olea, P. P. (2025). Farmland abandonment and season drive scavenging dynamics in livestock-rewilded landscapes. Ecological Applications, 35(8), e70151. https://doi.org/10.1002/eap.70151
DeVault, T. L., & Rhodes, O. E. (2002). Identification of vertebrate scavengers of small mammal carcasses in a forested landscape. Acta Theriologica, 47(2), 185–192. https://doi.org/10.1007/BF03192458
DeVault, T. L., Rhodes, O. E., & Shivik, J. A. (2003). Scavenging by vertebrates: Behavioral, ecological, and evolutionary perspectives on an important energy transfer pathway in terrestrial ecosystems. Oikos, 102(2), 225–234. https://doi.org/10.1034/j.1600-0706.2003.12378.x
DeVault, T., Brisbin, J., & Rhodes, O. (2004). Factors influencing the acquisition of rodent carrion by vertebrate scavengers and decomposers. Canadian Journal of Zoology, 82. https://doi.org/10.1139/z04-022
Enari, H., & Enari, H. S. (2021). Not avian but mammalian scavengers efficiently consume carcasses under heavy snowfall conditions: A case from northern Japan. Mammalian Biology, 101(4), 419–428. https://doi.org/10.1007/s42991-020-00097-9
Fahrig, L., Baudry, J., Brotons, L., Burel, F. G., Crist, T. O., Fuller, R. J., … Martin, J. -L. (2011). Functional landscape heterogeneity and animal biodiversity in agricultural landscapes. Ecology Letters, 14(2), 101–112. https://doi.org/10.1111/j.1461-0248.2010.01559.x
Fayet, C. M. J., Reilly, K. H., Van Ham, C., & Verburg, P. H. (2022). What is the future of abandoned agricultural lands? A systematic review of alternative trajectories in Europe. Land Use Policy, 112, 105833. https://doi.org/10.1016/j.landusepol.2021.105833
Fischer, J., Hartel, T., & Kuemmerle, T. (2012). Conservation policy in traditional farming landscapes. Conservation Letters, 5(3), 167–175. https://doi.org/10.1111/j.1755-263X.2012.00227.x
Frei, T., Espelta, J. M., Górriz-Mifsud, E., Hampe, A., Lefèvre, F., Martín-Forés, I., & Winkel, G. (2024). Can natural forest expansion contribute to Europe’s restoration policy agenda? An interdisciplinary assessment. Ambio, 53(1), 34–45. https://doi.org/10.1007/s13280-023-01924-2
García, D., Suárez-Seoane, S., Jiménez-Alfaro, B., Álvarez, D., Álvarez-Álvarez, P., Álvarez-Martínez, J. M., … Santín, C. (2023). Renaturalización pasiva en la Cordillera Cantábrica: bases y retos científicos para una sostenibilidad socio-ecológica. Ecosistemas, 32(1), 2507. https://doi.org/10.7818/ECOS.2507
Hsieh, T. C., Ma, K. H., & Chao, A. (2016). iNEXT: An R package for rarefaction and extrapolation of species diversity (Hill numbers). Methods in Ecology and Evolution, 7(12), 1451–1456. https://doi.org/10.1111/2041-210X.12613
Hsieh, T. C., Ma, K. H., & Chao, A. (2024). iNEXT: Interpolation and extrapolation for species diversity (Version 3.0.1) [R package]. Retrieved July 2025 from https://cran.r-project.org/package=iNEXT
Jost, L. (2006). Entropy and diversity. Oikos, 113(2), 363–375. https://doi.org/10.1111/j.2006.0030-1299.14714.x
Jost, L. (2007). Partitioning diversity into independent alpha and beta components. Ecology, 88(10), 2427–2439. https://doi.org/10.1890/06-1736.1
MacDonald, D., Crabtree, J. R., Wiesinger, G., Dax, T., Stamou, N. Fleury, P., … Gibon, A. (2000). Agricultural abandonment in mountain areas of Europe: Environmental consequences and policy response. Journal of Environmental Management, 59(1), 47–69. https://doi.org/10.1006/jema.1999.0335
Martin-Díaz, P., Cortés-Avizanda, A., Serrano, D., Arrondo, E., Sánchez-Zapata, J. A., & Donázar, J. A. (2020). Rewilding processes shape the use of Mediterranean landscapes by an avian top scavenger. Scientific Reports, 10(1). https://doi.org/10.1038/s41598-020-59591-2
Mateo-Tomás, P., Olea, P. P., Moleón, M., Vicente, J., Botella, F., Selva, N., … Sánchez-Zapata, J. A. (2015). From regional to global patterns in vertebrate scavenger communities subsidized by big game hunting. Diversity and Distributions, 21(8), 913–924. https://doi.org/10.1111/ddi.12330
Mateo-Tomás, P., Olea, P. P., Moleón, M., Selva, N., & Sánchez-Zapata, J. A. (2017). Both rare and common species support ecosystem services in scavenger communities. Global Ecology and Biogeography, 26(12), 1459–1470. https://doi.org/10.1111/geb.12673
Mateo-Tomás, P., Olea, P. P., Selva, N., & Sánchez-Zapata, J. A. (2019). Species and individual replacements contribute more than nestedness to shape vertebrate scavenger metacommunities. Ecography, 42(2), 365–375. https://doi.org/10.1111/ecog.03854
Moleón, M., Sánchez-Zapata, J. A., Margalida, A., Carrete, M., Owen-Smith, N., & Donázar, J. A. (2014). Humans and scavengers: The evolution of interactions and ecosystem services. BioScience, 64(5), 394–403. https://doi.org/10.1093/biosci/biu034
Moleón, M., Sánchez-Zapata, J. A., Sebastián-González, E., & Owen-Smith, N. (2015). Carcass size shapes the structure and functioning of an African scavenging assemblage. Oikos, 124(10), 1391–1403. https://doi.org/10.1111/oik.02222
Morales-Reyes, Z., Sánchez-Zapata, J. A., Sebastián-González, E., Botella, F., Carrete, M., & Moleón, M. (2017). Scavenging efficiency and red fox abundance in Mediterranean mountains with and without vultures. Acta Oecologica, 79, 81–88. https://doi.org/10.1016/j.actao.2016.12.012
Mougeot, F., García, J. T., & Viñuela, J. (2009). Biología reproductora, comportamiento y conservación del milano real (Milvus milvus), con especial énfasis en las poblaciones mediterráneas. SEO/BirdLife. Informe técnico.
Mutillod, C., Buisson, É., Mahy, G., Jaunatre, R., Bullock, J. M., Tatin, L., & Dutoit, T. (2024). Ecological restoration and rewilding: Two approaches with complementary goals? Biological Reviews, 99(3), 820–836. https://doi.org/10.1111/brv.13046
Ogada, D. L., Torchin, M. E., Kinnaird, M. F., & Ezenwa, V. O. (2012). Effects of vulture declines on facultative scavengers and potential implications for mammalian disease transmission. Conservation Biology, 26(3), 453–460. https://doi.org/10.1111/j.1523-1739.2012.01827.x
Oh, H. S., Baek, I. S., Kim, N. Y., & Park, S. H. (2024). Influence of carcass mass on decomposition rate: A medico-legal entomology perspective. Entomological Research, 54(2), e12705. https://doi.org/10.1111/1748-5967.12705
Oksanen, J., Simpson, G. L., Blanchet, F. G., Kindt, R., Legendre, P., Minchin, P. R. ... Weedon, J. (2025). vegan: Community ecology package (Version 2.6-6) [R package]. Retrieved July 2025 from https://cran.r-project.org/package=vegan
Olea, P. P., Mateo-Tomás, P., & Sánchez-Zapata, J. A. (Eds.). (2019). Carrion ecology and management (Vol. 2). Springer International Publishing. https://doi.org/10.1007/978-3-030-16501-7
Olea, P. P., Fernández-García, M., López-Bao, J. V., Viñuela, J., Valente e Santos, J. P., Rodríguez-Pérez, J., … Mateo-Tomás, P. (2022). Unraveling the real magnitude of illegal wildlife poisoning to halt cryptic biodiversity loss. Biological Conservation, 273, 109702. https://doi.org/10.1016/j.biocon.2022.109702
Oliva-Vidal, P., Sebastián-González, E., & Margalida, A. (2022). Scavenging in changing environments: Woody encroachment shapes rural scavenger assemblages in Europe. Oikos, 2022(12), e09310. https://doi.org/10.1111/oik.09310
Oñate, J. J., Acebes, P., & Olea, P. P. (2023). Aprender del pasado para afrontar el futuro: Desafíos ambientales de la agricultura española en el siglo XXI: Una mirada desde el legado de Fernando González Bernáldez. Ecosistemas, 32(especial), 2495. https://doi.org/10.7818/ECOS.2495
Oppermann, R., Beaufoy, G., & Jones, G. (Eds.). (2012). High nature value farming in Europe: 35 European countries – Experiences and perspectives. Verlag Regionalkultur. ISBN: 978-3-89735-657-3
Pardo-Barquín, E., Mateo-Tomás, P., & Olea, P. P. (2019). Habitat characteristics from local to landscape scales combine to shape vertebrate scavenging communities. Basic and Applied Ecology, 34, 126–139. https://doi.org/10.1016/j.baae.2018.08.005
Pereira, H. M., & Navarro, L. M. (Eds.). (2015). Rewilding European landscapes. Springer International Publishing. https://doi.org/10.1007/978-3-319-12039-3
Perino, A., Pereira, H. M., Navarro, L. M., Fernández, N., & Wheeler, H. C. (2019). Rewilding complex ecosystems. Science, 364(6438), eaav5570. https://doi.org/10.1126/science.aav5570
Pettorelli, N., Barlow, J., Stephens, P. A., et al. (2018). Making rewilding fit for policy. Journal of Applied Ecology, 55(3), 1114–1125. https://doi.org/10.1111/1365-2664.13082
Plieninger, T., Höchtl, F., & Spek, T. (2006). Traditional land-use and nature conservation in European rural landscapes. Environmental Science & Policy, 9(4), 317–321. https://doi.org/10.1016/j.envsci.2006.03.001
Plieninger, T., Draux, H., Fagerholm, N., Bieling, C., Bürgi, M., Kizos, T., … Verburg, P. H. (2016). The driving forces of landscape change in Europe: A systematic review of the evidence. Land Use Policy, 57, 204–214. https://doi.org/10.1016/j.landusepol.2016.04.040
Queiroz, C., Beilin, R., Folke, C., & Lindborg, R. (2014). Farmland abandonment: Threat or opportunity for biodiversity conservation? A global review. Frontiers in Ecology and the Environment, 12(5), 288–296. https://doi.org/10.1890/120348
R Core Team. (2025). R: Un lenguaje y entorno para el análisis estadístico y la generación de gráficos. R Foundation for Statistical Computing. https://www.r-project.org/
Romero, A. (2020). The fate of small-mammal carrion is affected by carcass size and visual conspicuousness in a Neotropical rainforest. Therya, 11(3), 423–431. https://doi.org/10.12933/therya-20-988
Ruxton, G. D., & Houston, D. C. (2004). Obligate vertebrate scavengers must be large soaring fliers. Journal of Theoretical Biology, 228(3), 431-436. https://doi.org/10.1016/j.jtbi.2004.02.005
Schuh, B., GmbH, Ö., Andronic, C., Derszniak-Noirjean, M., Gaupp-Berghausen, M., Hsiung, C. H., … Brkanovic, S. (2020). Research for AGRI Committee—The challenge of land abandonment after 2020 and options for mitigating measures. European Parliament, Policy Department for Structural and Cohesion Policies. Retrieved July 2025 from https://www.europarl.europa.eu/RegData/etudes/STUD/2020/652238/IPOL_STU(2020)652238_EN.pdf
Sebastián-González, E., Sánchez-Zapata, J. A., Donázar, J. A., Selva, N., Cortés-Avizanda, A., Hiraldo, F., … Moleón, M. (2013). Interactive effects of obligate scavengers and scavenger community richness on lagomorph carcass consumption patterns. Ibis, 155(4), 881–885. https://doi.org/10.1111/ibi.12079
Sebastián-González, E., Moleón, M., Gibert, J. P., Botella, F., Mateo-Tomás, P., Olea, P. P., … Sánchez-Zapata, J. A. (2016). Nested species-rich networks of scavenging vertebrates support high levels of interspecific competition. Ecology, 97(1), 95–105. https://doi.org/10.1890/15-0212.1
Sebastián-González, E., Morales-Reyes, Z., Botella, F., Naves-Alegre, L., Pérez-García, J. M., Mateo-Tomás, P., … Sánchez-Zapata, J. A. (2021). Functional traits driving species role in the structure of terrestrial vertebrate scavenger networks. Ecology, 102(12), e03519. https://doi.org/10.1002/ecy.3519
Selva, N., Jędrzejewska, B., Jedrzejewski, W., & Wajrak, A. (2005). Factors affecting carcass use by a guild of scavengers in European temperate woodland. Canadian Journal of Zoology, 83, 1590–1601. https://doi.org/10.1139/z05-158
Socolar, J. B., Gilroy, J. J., Kunin, W. E., & Edwards, D. P. (2016). How should beta-diversity inform biodiversity conservation? Trends in Ecology & Evolution, 31(1), 67–80. https://doi.org/10.1016/j.tree.2015.11.005
Spencer, E. E., Dickman, C. R., Greenville, A., Barton, P., & Newsome, T. M. (2024). Vertebrate scavenging in Australia is shaped by a complex interplay of bioregional, seasonal and habitat factors. Journal of Zoology, 324, 128–140. https://doi.org/10.1111/jzo.13200
Svenning, J. C., Pedersen, P. B. M., Donlan, C. J., Ejrnæs, R., Faurby, S., Galetti, M., … Vera, F. W. M. (2016). Science for a wilder Anthropocene: Synthesis and future directions for trophic rewilding research. Proceedings of the National Academy of Sciences, 113(4), 898–906. https://doi.org/10.1073/pnas.1502556112
Torre, I., Díaz, M., Martínez-Padilla, J., Bonal, R., Viñuela, J., & Fargallo, J. A. (2007). Cattle grazing, raptor abundance and small mammal communities in Mediterranean grasslands. Basic and Applied Ecology, 8, 565–575. https://doi.org/10.1016/j.baae.2006.09.016
Turner, K. L., Abernethy, E. F., Conner, L. M., Rhodes, O. E., & Beasley, J. C. (2017). Abiotic and biotic factors modulate carrion fate and vertebrate scavenging communities. Ecology, 98(9), 2413–2424. https://doi.org/10.1002/ecy.1930
Ustaoglu, E., & Collier, M. J. (2018). Farmland abandonment in Europe: An overview of drivers, consequences, and assessment of the sustainability implications. Environmental Reviews, 26(4), 396–416. https://doi.org/10.1139/er-2018-0001
Whittaker, R. H. (1960). Vegetation of the Siskiyou Mountains, Oregon and California. Ecological Monographs, 30(3), 279–338. https://doi.org/10.2307/1943563
Wilson, E. E., & Wolkovich, E. M. (2011). Scavenging: How carnivores and carrion structure communities. Trends in Ecology & Evolution, 26, 129–135. https://doi.org/10.1016/j.tree.2010.12.011
Anexo / Appendix
Características de los puntos de muestreo
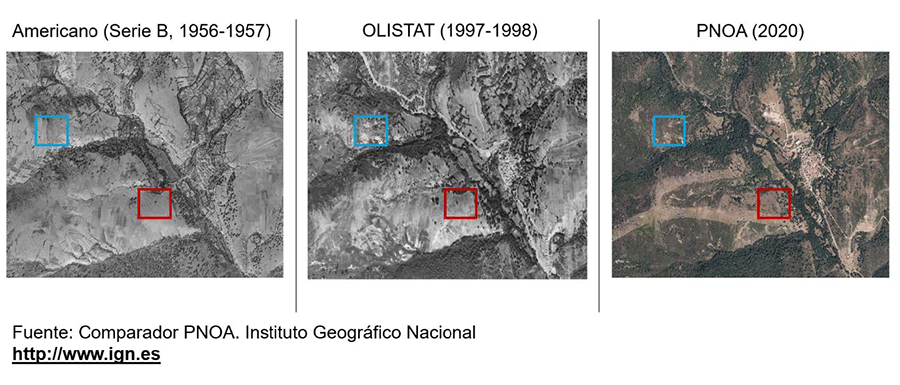
Figura A1. Serie de ortofotos históricas (años 1956, 1997 y 2020) que ilustran la progresiva transformación del paisaje tras el abandono de la ganadería extensiva en una de las zonas del área de estudio (Puebla de la Sierra, norte de la Comunidad de Madrid). Los recuadros azules señalan áreas anteriormente pastoreadas y abiertas que muestran actualmente claros signos de abandono y regeneración de vegetación leñosa; los recuadros rojos corresponden a áreas también pastoreadas en el pasado, pero que mantienen la actividad ganadera en la actualidad.
Figure A1. Series of historical orthophotos (years 1956, 1997, and 2020) illustrating the progressive landscape transformation following extensive livestock grazing abandonment in one region within the study areas (Puebla de la Sierra, northern Madrid region, Spain). Blue boxes represent plots that were grazed and open, which now show clear signs of abandonment and woody vegetation encroachment; red boxes correspond to areas also grazed in the past but where grazing activity is still maintained today.
Nota: La selección de parcelas se realizó en dos fases: (i) análisis de ortofotos históricas (desde 1956 hasta el PNOA de 2020) para identificar áreas utilizadas en el pasado para pastoreo y su evolución hacia hábitats más cerrados tras el abandono, y (ii) verificación en campo para seleccionar y emparejar las parcelas definitivas. Así, cada par de parcelas representaba etapas sucesivas de la misma trayectoria de uso del suelo y sucesión ecológica. Por ejemplo, las dehesas de encina, moldeadas por el uso ganadero, se emparejaron con bosques de encina más cerrados que se desarrollaron a partir de esas dehesas tras su abandono.
La distancia media entre parcelas emparejadas fue de 2.6 km (rango: 1.1–6.1 km), un rango elegido para minimizar la probabilidad de registrar los mismos individuos de especies necrófagas en ambos tipos de hábitat y garantizar independencia espacial. Estas distancias se seleccionaron a partir de estimas de área de campeo disponibles para la mayoría de las especies necrófagas de pequeño y mediano tamaño presentes en el área de estudio, como el zorro (Vulpes vulpes) y las martas (Martes spp). Por ejemplo, los zorros suelen ocupar áreas de campeo de 2–6 km² (Cavallini, 1996; Dekker et al., 2001), mientras que las martas muestran patrones de movimiento similares (Wereszczuk y Zalewski, 2019; Zalewski et al., 2004). Este protocolo espacial fue desarrollado en un estudio previo (Olea et al., 2022), donde se utilizaron cebos de pollo colocados a 1–3 km de distancia dentro de las áreas de estudio para asegurar la independencia de las muestras en función de la ecología de movimiento de los carroñeros terrestres. Nuestro diseño actual replica ese enfoque, con distancias medias entre parcelas dentro de esos márgenes. Por ejemplo, asumiendo áreas de campeo circulares, dos individuos con rangos de 1.5 km de radio (~7 km² cada uno) se solaparían en ~50 % si sus centros estuvieran separados 1.5 km. A 3 km de separación—ligeramente superior a nuestra media—no existiría solapamiento. Esta separación minimiza la probabilidad de registrar repetidamente a los mismos individuos en diferentes parcelas y refuerza así la independencia estadística
Si bien es cierto que algunas especies de amplio rango de movimiento (p. ej., buitres, águilas, milanos) cubren distancias mucho mayores, su presencia en las carroñas difirió de forma consistente entre tipos de hábitat, lo que refleja más bien preferencias asociadas a las condiciones del hábitat que un mero solapamiento espacial. En definitiva, además de garantizar cierta independencia espacial mediante la distancia media seleccionada, nuestro objetivo fue elegir parcelas pareadas ambientalmente similares que difiriesen principalmente en la presencia o ausencia de pastoreo. Este enfoque nos permitió atribuir las diferencias observadas a procesos ecológicos secundarios derivados del cese de la actividad ganadera.

Figura A2. Ejemplos de parcelas pastoreadas (arriba) y parcelas abandonadas (abajo) incluidas en el estudio. Las imágenes ilustran la heterogeneidad de microhábitat dentro de cada tipo de hábitat. En los hábitats pastoreados predominan pastizales abiertos y dehesas con escaso sotobosque, presentando una cobertura arbórea media del 15.5 % y arbustiva del 19 %. En contraste, los hábitats abandonados muestran signos de sucesión secundaria avanzada, con un incremento de la cobertura arbustiva (61 %) y arbórea (51 %), incluyendo matorrales de bajo (<1 m) y alto porte (>1 m). Aunque todas las parcelas abandonadas reflejan un abandono prolongado, existe cierta heterogeneidad en la cobertura vegetal entre ellas. Autores de las fotos: P.P. Olea, Iván Herranz y R.R. Daza.
Figure A2.
Examples of grazed (above) and abandoned plots (below) included in the study.
The photographs illustrate the microhabitat heterogeneity within each habitat
type. In grazed habitats, open grasslands and “dehesas” with sparse woody
vegetation predominate, with an average forest cover of 15.5 % and shrub cover
of 19 %. In contrast, abandoned habitats show signs of advanced secondary
succession, with increased shrub (61 %) and forest cover (51 %), including low
(<1 m) and tall (>1 m) shrubs. Although all abandoned plots reflect
progressive abandonment, there is some heterogeneity in vegetation cover among
them. Photo credits: P.P. Olea, Iván Herranz and R.R. Daza.
Tabla A1. Características de los puntos de muestreo (localización y tipo de hábitat), de las carroñas utilizadas (pollos enteros y con plumas) y de las fechas y horas de instalación de las cámaras de fototrampeo en la vertiente sur de la Sierra de Guadarrama (Madrid, España).
Table A1. Characteristics of the sampling sites (location and habitat type), the carrion used (whole feathered chickens), and the dates and times of camera-trap installation on the southern slope of the Sierra de Guadarrama (Madrid, Spain).
|
Punto |
Lugar |
Tipo de hábitat |
Peso (g) |
Fecha y hora instalación |
|
1 |
Cerceda - Colmenar Viejo |
Abandonado |
560 |
11/07/2022 10:40 |
|
2 |
Colmenar Viejo |
Pastoreado |
990 |
11/07/2022 12:15 |
|
3 |
Cerceda |
Abandonado |
1000 |
11/07/2022 9:32 |
|
4 |
Cerceda - Colmenar Viejo |
Pastoreado |
300 |
11/07/2022 8:45 |
|
5 |
Pedrezuela (Montenebro) |
Abandonado |
730 |
13/06/2022 10:25 |
|
6 |
Pedrezuela (Montenebro) |
Pastoreado |
800 |
13/06/2022 11:30 |
|
7 |
Guadalix |
Abandonado |
540 |
13/06/2022 8:41 |
|
8 |
Guadalix |
Pastoreado |
1260 |
18/07/2022 11:55 |
|
9 |
Miraflores-Morcuera |
Abandonado |
860 |
13/06/2022 13:40 |
|
10 |
Bustarviejo |
Pastoreado |
750 |
13/06/2022 15:30 |
|
11 |
Valdemanco |
Abandonado |
960 |
13/06/2022 21:21 |
|
12 |
Valdemanco |
Pastoreado |
760 |
13/06/2022 19:16 |
|
13 |
Bustarviejo |
Abandonado |
790 |
13/06/2022 17:50 |
|
14 |
Bustarviejo |
Pastoreado |
920 |
13/06/2022 16:44 |
|
15 |
Colmenar Viejo |
Pastoreado |
1320 |
11/07/2022 13:50 |
|
16 |
Valdemanco |
Abandonado |
820 |
13/06/2022 20:30 |
|
17 |
Valdemanco |
Pastoreado |
700 |
13/06/2022 22:19 |
|
18 |
Puebla de la Sierra |
Abandonado |
730 |
04/07/2022 13:15 |
|
19 |
Puebla de la Sierra |
Pastoreado |
990 |
04/07/2022 12:15 |
|
20 |
Robledillo de la Jara |
Abandonado |
780 |
04/07/2022 8:20 |
|
21 |
Robledillo de la Jara |
Pastoreado |
620 |
04/07/2022 7:35 |
|
22 |
Colmenar Viejo |
Abandonado |
720 |
11/07/2022 19:30 |
|
23 |
Colmenar Viejo |
Pastoreado |
930 |
11/07/2022 18:45 |
|
24 |
Puebla de la Sierra |
Abandonado |
870 |
04/07/2022 14:20 |
|
25 |
Puebla de la Sierra |
Pastoreado |
880 |
04/07/2022 16:45 |
|
26 |
Robledillo de la Jara |
Abandonado |
760 |
04/07/2022 9:25 |
|
27 |
Puebla de la Sierra |
Pastoreado |
990 |
04/07/2022 10:50 |
|
28 |
Puebla de la Sierra |
Abandonado |
960 |
21/07/2022 12:25 |
|
29 |
Puebla de la Sierra |
Pastoreado |
860 |
04/07/2022 21:00 |
|
30 |
Guadalix |
Pastoreado |
890 |
18/07/2022 13:10 |
|
31 |
Horcajuelo de la Sierra |
Abandonado |
630 |
27/06/2022 16:52 |
|
32 |
Horcajo de la Sierra |
Pastoreado |
890 |
27/06/2022 16:00 |
|
33 |
Robregordo - La Acebeda |
Abandonado |
880 |
27/06/2022 10:40 |
|
34 |
Horcajo de la Sierra |
Pastoreado |
800 |
27/06/2022 14:20 |
|
35 |
La Acebeda |
Abandonado |
910 |
27/06/2022 11:35 |
|
36 |
La Acebeda - Braojos |
Pastoreado |
710 |
27/06/2022 12:30 |
|
37 |
Somosierra |
Abandonado |
740 |
27/06/2022 8:50 |
|
38 |
Somosierra |
Pastoreado |
800 |
27/06/2022 8:00 |
|
39 |
Puebla de la Sierra |
Abandonado |
790 |
04/07/2022 19:50 |
|
40 |
Puebla de la Sierra |
Pastoreado |
970 |
04/07/2022 18:15 |
|
41 |
Montejo de la Sierra |
Abandonado |
720 |
27/6/2022 18_10 |
|
42 |
Montejo de la Sierra |
Pastoreado |
790 |
27/06/2022 17:40 |
|
43 |
Robregordo |
Abandonado |
780 |
27/06/2022 9:45 |
|
44 |
Horcajo de la Sierra |
Pastoreado |
810 |
27/06/2022 13:19 |
|
45 |
Pedrezuela |
Abandonado |
970 |
18/07/2022 15:20 |
|
46 |
San Agustín de Guadalix |
Abandonado |
540 |
18/07/2022 17:00 |
|
47 |
San Agustín de Guadalix |
Pastoreado |
840 |
18/07/2022 18:45 |
|
48 |
Colmenar Viejo |
Abandonado |
590 |
11/07/2022 7:20 |
|
49 |
Hoyo de Manzanares |
Abandonado |
820 |
11/07/2022 16:45 |
|
50 |
Hoyo de Manzanares |
Abandonado |
1020 |
11/07/2022 17:20 |
|
51 |
Colmenar Viejo |
Pastoreado |
890 |
11/07/2022 6:30 |
|
52 |
Colmenar Viejo |
Pastoreado |
840 |
11/07/2022 15:50 |
Nota: El paisaje presenta una elevada heterogeneidad estructural y florística como resultado de una larga historia de manejo ganadero y procesos recientes de renaturalización. Los principales usos del suelo en el área de estudio corresponden a tipos de hábitat recogidos en el Anexo I de la Directiva Hábitats (92/43/CEE), entre los que destacan: Pastizales: Incluyen extensiones abiertas dominadas por especies herbáceas anuales y perennes, con presencia destacada del hábitat prioritario 6220 (Zonas subestépicas de gramíneas y anuales del Thero-Brachypodietea). Dehesas: Sistemas agrosilvopastorales seminaturales clasificados como hábitat 6310 (Dehesas perennifolias de Quercus spp.), con cobertura dispersa de árboles y uso ganadero activo o histórico. Matorrales: Principalmente jarales (Cistus ladanifer), aunque también se incluyen otros tipos como el hábitat 5210 (Matorrales arborescentes de Juniperus spp.), 4030 (Brezales secos europeos) y 4090 (Brezales oromediterráneos endémicos con aliaga). Bosques esclerófilos mediterráneos: Representados por hábitats 9340 (Encinares de Quercus ilex y Q. rotundifolia) y 9380 (Bosques de Ilex aquifolium). Bosques caducifolios: Entre ellos se encuentran el hábitat 91B0 (Fresnedas termófilas de Fraxinus angustifolia) y 9230 (Robledales galaico-portugueses con Quercus robur y Q. pyrenaica). Por motivos metodológicos, se excluyeron del estudio las masas forestales dominadas por pino silvestre (Pinus sylvestris).
Completitud de muestra
Tabla A2. Valores de completitud de muestra (sample completeness) obtenidos a partir de datos recolectados en carroñas ubicadas en dos tipos de hábitats: pastoreado y abandonado. La completitud de muestra se estima para distintos órdenes de diversidad q, lo que permite evaluar la representatividad de las muestras en función de la sensibilidad a especies raras o comunes. Para cada valor de q, se incluye el valor estimado de completitud junto con su intervalo de confianza al 95% (límites inferior y superior), lo que proporciona una medida de la precisión de las estimaciones.
Table A2. Sample completeness values obtained from data collected at carrion sites located in two habitat types: grazed and abandoned. Sample completeness is estimated for different diversity orders q, allowing the assessment of sample representativeness based on sensitivity to rare or common species. For each q value, the estimated completeness is reported along with its 95% confidence interval (lower and upper bounds), providing a measure of the precision of the estimates.
|
Hábitat pastoreado/ Grazed habitat |
|||
|
Orden q |
SC estimado |
SC LCL (IC 95 %) |
SC UCL (IC 95 %) |
|
0.0 |
0.3279124 |
0.00000000 |
0.6828219 |
|
0.2 |
0.4145785 |
0.08998381 |
0.7391733 |
|
0.4 |
0.5341614 |
0.26270879 |
0.805614 |
|
0.6 |
0.6700713 |
0.47140292 |
0.8687396 |
|
0.8 |
0.7935381 |
0.67015599 |
0.9169203 |
|
1.0 |
0.8841467 |
0.81788062 |
0.9504128 |
|
1.2 |
0.9402074 |
0.90625286 |
0.974162 |
|
1.4 |
0.9709524 |
0.95195824 |
0.9899466 |
|
1.6 |
0.9865012 |
0.97460868 |
0.9983938 |
|
1.8 |
0.9939381 |
0.98618523 |
1.00000000 |
|
2.0 |
0.9973519 |
0.9923208 |
1.00000000 |
|
Hábitat abandonado/ Abandoned habitat |
|||
|
0.0 |
0.7716895 |
0.4483643 |
1.00000000 |
|
0.2 |
0.8081383 |
0.5370599 |
1.00000000 |
|
0.4 |
0.8467382 |
0.6395013 |
1.00000000 |
|
0.6 |
0.8840917 |
0.7426606 |
1.00000000 |
|
0.8 |
0.9169839 |
0.8309621 |
1.00000000 |
|
1.0 |
0.9434389 |
0.8956026 |
0.9912752 |
|
1.2 |
0.9630756 |
0.9375167 |
0.9886346 |
|
1.4 |
0.9767142 |
0.9625994 |
0.9908291 |
|
1.6 |
0.9857049 |
0.9770125 |
0.9943973 |
|
1.8 |
0.9914013 |
0.9853606 |
0.997442 |
|
2.0 |
0.994906 |
0.9904108 |
0.9994012 |
Tabla A3. Listado de especies de vertebrados necrófagos registradas en el estudio, clasificadas según su gremio funcional. Se muestran los valores correspondientes a la suma total de individuos detectados en hábitats pastoreados y abandonados.
Table A3. List of scavenger vertebrate species recorded in the study, classified according to their functional guild. The values shown correspond to the total number of individuals detected in grazed and abandoned habitats.
|
Especie |
Gremio funcional |
Pastoreado |
Abandonado |
|
Buitre negro (Aegypius monachus) |
Obligado |
5 |
0 |
|
Águila imperial (Aquila adalberti) |
Facultativo: Depredador: Apical |
1 |
0 |
|
Azor común (Accipiter gentilis) |
Facultativo: Mesodepredador: Rapaz |
1 |
0 |
|
Milano negro (Milvus migrans) |
Facultativo: Mesodepredador: Rapaz |
5 |
0 |
|
Milano real (Milvus milvus) |
Facultativo: Mesodepredador: Rapaz |
9 |
4 |
|
Busardo ratonero (Buteo buteo) |
Facultativo: Mesodepredador: Rapaz |
1 |
1 |
|
Arrendajo (Garrulus glandarius) |
Facultativo: Omnívoro: Córvido |
2 |
4 |
|
Corneja (Corvus corone) |
Facultativo: Omnívoro: Córvido |
14 |
1 |
|
Cuervo (Corvus corax) |
Facultativo: Omnívoro: Córvido |
1 |
0 |
|
Rabilargo (Cyanopica cooki) |
Facultativo: Omnívoro: Córvido |
8 |
6 |
|
Urraca (Pica pica) |
Facultativo: Omnívoro: Córvido |
9 |
0 |
|
Garduña (Martes foina) |
Facultativo: Mesodepredador: Carnívoro |
6 |
14 |
|
Gineta (Genetta genetta) |
Facultativo: Mesodepredador: Carnívoro |
1 |
2 |
|
Jabali (Sus scrofa) |
Facultativo: Omnívoro: Mamífero |
15 |
61 |
|
Perro (Canis l. familiaris) |
Facultativo: Omnívoro: Mamífero |
1 |
1 |
|
Ratón (Apodemus sp) |
Facultativo: Omnívoro: Mamífero |
1 |
6 |
|
Tejon (Meles meles) |
Facultativo: Mesodepredador: Carnívoro |
6 |
3 |
|
Zorro (Vulpes vulpes) |
Facultativo: Mesodepredador: Carnívoro |
38 |
35 |
|
Culebra bastarda (Malpolon monspessulanus) |
Facultativo: Omnívoro: Reptil |
1 |
1 |
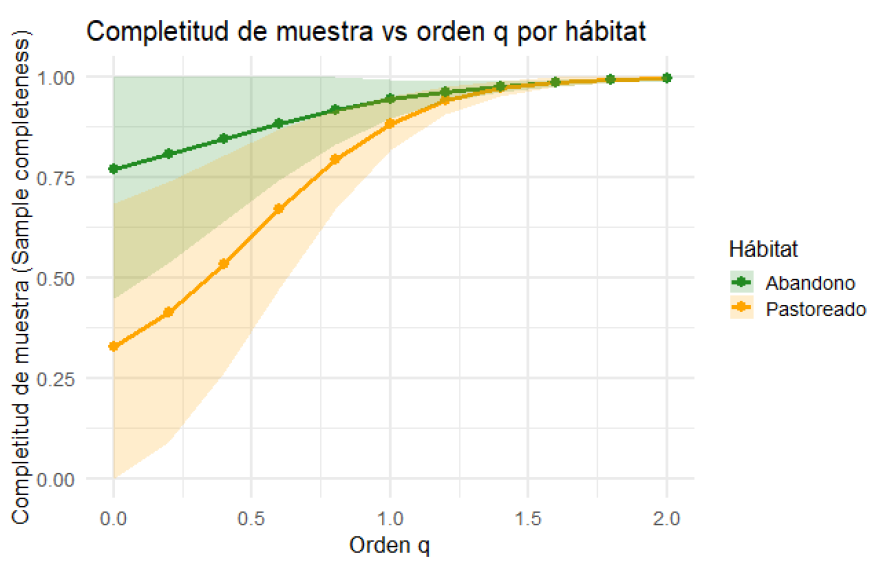
Figura A3. Completitud de muestra (sample completeness) en función del orden q de diversidad para cada tipo de hábitat: abandonados (verde) y pastoreados (naranja), considerando diferentes sensibilidades a especies raras (q = 0), comunes (q = 1) y dominantes (q = 2). Las áreas sombreadas se corresponden con los intervalos de confianza al 95% para cada estimación.
Figure A3. Sample completeness as a function of diversity order q for each habitat type: abandoned (green) and grazed (orange), reflecting different sensitivity to rare (q = 0), common (q = 1), and dominant (q = 2) species. Shaded areas represent 95% confidence intervals for each estimate.
Referencias del Anexo
Cavallini, P. 1996. Variation in the social system of the red fox. Ethology Ecology & Evolution, 8: 323–342. https://doi.org/10.1080/08927014.1996.9522906
Dekker, J. J. A., Stein, A., & Heitkönig, I. M. A. 2001. A spatial analysis of a population of red fox (Vulpes vulpes) in the Dutch coastal dune area. Journal of Zoology, 255: 505–510. https://doi.org/10.1017/S0952836901001583
Olea, P. P., Fernández-García, M., López-Bao, J. V., Vinuela, J., e Santos, J. P. V., Rodríguez-Pérez, J., ... & Mateo-Tomás, P. (2022). Unraveling the real magnitude of illegal wildlife poisoning to halt cryptic biodiversity loss. Biological Conservation, 273, 109702. https://doi.org/10.1016/j.biocon.2022.109702
Wereszczuk, A., & Zalewski, A. 2019. Does the matrix matter? Home range sizes and space use strategies in stone marten at sites with differing degrees of isolation. Mammal Research, 64: 71–85. https://doi.org/10.1007/s13364-018-0397-6
Zalewski, A., Jędrzejewski, W., & Jędrzejewska, B. 2004. Mobility and home range use by pine martens (Martes martes) in a Polish primeval forest. Écoscience, 11: 113–122. https://doi.org/10.1080/11956860.2004.11682815