ecosistemas
ISSN 1697-2473
Open access / CC BY-NC 4.0
© 2026 Los autores [ECOSISTEMAS no se hace responsable del uso indebido de material sujeto a derecho de autor] / © 2026 The authors [ECOSISTEMAS is not responsible for the misuse of copyrighted material]
Ecosistemas 35(1): 2716 [enero - abril / January - April, 2026]: https://doi.org/10.7818/ECOS.2716
Editora asociado / Associate editor: José Manuel Álvarez-Martínez
ARTÍCULO DE INVESTIGACIÓN / RESEARCH ARTICLE
Caracterización dasométrica y diversidad de plantas vasculares en acebuchales de la isla de Menorca a lo largo de un gradiente de madurez
(1) Camí de Torret, 62. 07710. Sant Lluís, Menorca, Illes Balears, España.
* Autor de correspondencia / Corresponding author: M. Pons [marcpons2003@gmail.com]
|
> Recibido / Received: 26/02/2024 – Aceptado / Accepted: 20/01/2026 |
Cómo citar / How to cite: Pons Sintes, M. (2026). Caracterización dasométrica y diversidad de plantas vasculares en acebuchales de la isla de Menorca a lo largo de un gradiente de madurez. Ecosistemas 35(1): 2716. https://doi.org/10.7818/ECOS.2716
|
Caracterización dasométrica y diversidad de plantas vasculares en acebuchales de la isla de Menorca a lo largo de un gradiente de madurez Resumen: Los acebuchales son comunidades arborescentes dominadas por Olea europaea L. que constituyen los bosques más abundantes de la isla de Menorca, situada en el centro de la Cuenca del Mediterráneo Occidental. En este estudio se ha realizado una caracterización dasométrica y un estudio de la diversidad de plantas vasculares en acebuchales en función de su grado de madurez. Se estudiaron tres bosques con distinto grado de maduración en los que se seleccionaron parcelas al azar y se midieron una serie de parámetros dasométricos y de diversidad de especies. Los resultados indicaron que la espesura constituye un parámetro clave en el proceso de maduración. La espesura disminuye con la madurez, mientras que la comunidad arbórea se vuelve progresivamente más heterogénea. La gran capacidad de O. europaea como pionera en la formación de bosques primarios brinda la oportunidad ecológica necesaria para que otras especies se desarrollen. Los resultados obtenidos muestran que los procesos de maduración en los acebuchales se relacionan con una disminución de la espesura, un aumento de la equidad de especies en la comunidad arbórea y un aumento del número de fanerófitos en la comunidad de plantas vasculares. Estos resultados aportan indicadores estructurales y funcionales útiles para evaluar el estado de madurez de los acebuchales en paisajes mediterráneos. Palabras clave: equidad; espesura; madurez forestal; Olea europaea L.; sucesión vegetal Dasometric characterisation and vascular plant diversity in wild olive forests on the island of Menorca along a maturity gradient Abstract: The wild olive forests are arborescent communities dominated by Olea europaea L. that constitute the most abundant forests on the island of Menorca, located in the centre of the Western Mediterranean Basin. In this study, a dasometric characterisation and a study of the diversity of vascular plants in wild olive forests according to their degree of maturity was carried out. Three forests with different degrees of maturity were studied, from which plots were randomly selected and a series of dasometric and species diversity parameters were measured. The results indicated that density is a key parameter in the forest maturity gradient. Tree density decreases with maturity, while the tree community becomes more heterogeneous. The great capacity of O. europaea as a pioneer in the formation of primary forests provides the necessary ecological opportunity for other species to develop. The results obtained show that the maturation processes in wild olive forests are related to a decrease in density, an increase in evenness in the tree community, and an increase in the number of phanerophytes in the vascular plant community. These results provide structural and functional indicators to assess the maturity state of wild olive forests in Mediterranean landscapes. Keywords: density; evenness; forest maturity; Olea europaea L.; plant succession |
Introducción
El clima mediterráneo, la complejidad del territorio y el histórico uso de los suelos hacen del paisaje mediterráneo un sistema ecológico singular (Gómez Sal, 2008). La Cuenca Mediterránea es un punto caliente de biodiversidad (Médail y Quézel, 1999; Myers et al., 2000), si bien también es uno de los puntos calientes de cambio global. El cambio climático ocurre de manera más acelerada en la Cuenca Mediterránea respecto a la media global (Pausas y Millán, 2019). El cambio de uso del suelo también se está acelerando por la actividad humana, ya sea por la degradación de ecosistemas o por el abandono de la actividad agrícola tradicional (Gauquelin et al., 2018). Las Islas Baleares forman un archipiélago situado en el centro de la Cuenca Mediterránea Occidental, constituido por cuatro islas habitadas y cerca de un centenar de islotes con algún tipo de vegetación (Rita y Payeras, 2006). La isla de Menorca es la más oriental, con un catálogo de flora vascular formado por más de 1400 táxones, un número alto teniendo en cuenta la extensión y el gradiente altitudinal de la isla (Fraga et al., 2014). Según Fraga et al. (2004), los tres factores que determinan la diversidad vegetal de la isla de Menorca: el clima, la insularidad y la presencia humana. La vegetación predominantemente es de tipo esclerófilo seco debido a la distribución de precipitaciones que se concentran en el otoño, el carácter cárstico de sus suelos y el efecto desecante del viento (Fraga et al., 2004).
A pesar de las características climáticas e insulares, el paisaje vegetal de Menorca no se puede explicar sin tener en cuenta el papel que ha tenido la presencia humana en prácticamente toda la superficie de la isla (Fraga et al., 2014). El 52% de la isla corresponde a zonas forestales, el resto son zonas agrarias o artificiales. Las zonas forestales están en expansión por el abandono de los cultivos tradicionales, y en las Baleares han aumentado un 80% en los últimos 50 años (Ministerio de Agricultura, 1971; MITECO, 2020). La formación boscosa que ocupa una mayor superficie en Menorca es el acebuchal que abarcan el 48% de la superficie forestal de la isla (MITECO, 2020).
Los acebuchales son bosques donde predomina Olea europaea L. (Oleaceae), un árbol de hoja perenne, esclerófilo y polinizado por anemofilia (Kassout et al., 2019; Falek et al., 2022). Es un árbol de crecimiento lento que puede llegar a medir hasta 15-20 metros de altura, con tronco grisáceo y con ramas espinosas (Rey et al., 2009). O. europaea es una especie característica del paisaje mediterráneo, donde es un componente clave de los bosques y las maquias (Gianguzzi y Bazán, 2019). Es una de las principales especies fructífera durante el invierno en los paisajes mediterráneos floreciendo entre mayo y junio (Rey et al., 2009). La presencia de O. europaea en la región mediterránea se remonta al menos a la última glaciación y se considera un bioindicador del clima mediterráneo (Kassout et al., 2019).
Tal y como señala Fraga et al., 2014, la abundancia de O. europaea en un entorno como la Isla de Menorca se ve favorecida por el clima y los sustratos pobres que impiden el establecimiento de otras especies arbóreas, y factores humanos como el abandono de cultivos. O. europaea es una de las primeras plantas en crecer cuando se desarrolla una comunidad arborescente debido a sus características fisiológicas, que le permiten crecer en condiciones adversas para otras especies arbóreas (Gianguzzi y Bazán, 2019). Los acebuchales se han expandido en las Baleares en los últimos 50 años hasta un 425% (Ministerio de Agricultura, 1971; MITECO, 2020). Con todo esto, el resultado es un paisaje en forma de mosaico agroforestal donde O. europaea es el árbol dominante en gran parte de matorrales y bosques (Fraga et al., 2014).
El acebuchal sería la comunidad primaria dominante en ausencia de actividad agrícola, debido a que ya lo es en el mosaico agroforestal y en las zonas de cultivo abandonadas (Fraga et al., 2004). No obstante, el acebuchal no es una comunidad ecológicamente estable y corresponde a un estadio de la sucesión vegetal muy extendido por factores antrópicos que precede a la comunidad climácica de gran parte de la isla, el encinar (bosque de Quercus ilex L.) (Llorens et al., 2007). Los acebuchales están sujetos a procesos ecológicos como la maduración forestal y la sucesión ecológica. La madurez forestal implica una evolución de procesos ecológicos que llevan al avance y estancamiento temporal del ciclo de vida de los bosques en un estado maduro con árboles de avanzada edad y de mayor complejidad estructural (LIFE Red Bosques, 2020; Vayreda y Mezquida, 2020). La sucesión ecológica se define como un proceso dinámico y gradual de cambio de la estructura y composición de una comunidad vegetal a lo largo del tiempo hacia comunidades más estables (McIntosh, 1981; Chang y Turner, 2019). Los procesos de madurez forestal y sucesión ecológica ocurren simultáneamente e influyen en la dinámica de las comunidades arbóreas.
Algunas de las herramientas que se usan para estudiar la maduración y la sucesión forestal son la dasometría y la diversidad. La dasometría se refiere a la medición dimensional de ciertas características de los árboles, relativas a su forma o a la relación espacial entre individuos. La dasometría refleja las condiciones en las que han crecido el arbolado (Mostacedo y Fredericksen, 2000). Por otro lado, la diversidad es esencial para entender y medir el proceso de sucesión vegetal, ya que es en esencia un cambio en la composición de especies. Tanto la dasometría como la diversidad son aspectos clave en la comprensión de los procesos ecológicos de los bosques. A pesar de que la maduración se percibe como un proceso de cambio estructural y la sucesión como un proceso de cambio de diversidad, constituyen dos perspectivas complementarias de un mismo proceso. El objetivo de este estudio es evaluar cómo la madurez forestal y el avance sucesional modulan simultáneamente la estructura del arbolado y la diversidad de las comunidades de plantas vasculares en acebuchales de Menorca.
Material y métodos
Área de estudio
El estudio se realizó en la finca de Binisafúller d’en Moisi (39°50'50.2"N 4°13'46.7"E) situada en el municipio de Sant Lluís de la isla de Menorca (Islas Baleares, Cuenca del Mediterráneo Occidental; Fig. 1). La isla de Menorca tiene una superficie de 701.80 km2 y una altura máxima de 358 m.s.n.m. (Rosselló et al., 2003). El municipio de Sant Lluís se encuentra en la meseta meridional de Menorca que está en su totalidad formada por terreno terciario calcáreo. Forma una planicie situada a unos 50 metros sobre el nivel del mar sin relieves y solamente se halla surcado por algunos barrancos (Mercadal, 1962). El clima es mediterráneo con temperaturas cálidas en verano y no muy frías en invierno siendo la temperatura media de 17ºC. Presenta un diagrama ombrotérmico húmedo con una precipitación media de 573 mm al año siendo un régimen de lluvias de los más bajos de la isla (Jansà, 2004).
Diseño experimental. Establecimiento de parcelas de muestreo
Los diferentes sitios de muestreo se establecieron en función de la edad de los acebuchales. Para ello se recurrió a dos ortofotos de la Isla de Menorca que se presentan en la plataforma IDE Menorca tomadas en los años 1956 y 2015 (CIME, 2022; Infraestructura de Datos Espaciales de Menorca). Para definir bosques jóvenes y maduros se compararon ambas ortofotos considerándose la persistencia en el tiempo como un proxy de la madurez ecológica, asumiendo que bosques con mayor continuidad histórica han experimentado procesos más prolongados de maduración y sucesión. Fueron considerados jóvenes los que no estuvieran formados en 1956 pero sí en 2015, mientras que los maduros ya estarían formados en 1956. Al estudiar bosques muy próximos geográficamente eliminamos la variabilidad debida a distintas condiciones ambientales. Se ha comprobado que no ha habido ninguna intervención de manejo forestal en los últimos 50 años (Guardia-Camps, Comunicación Personal, 28 de junio de 2022).
Se seleccionaron tres bosques por las características mencionadas (Fig. 1). El primero de ellos (“Antiguo Cultivo”, Fig. 1, punto 1) fue anteriormente un campo de cultivo de Ceratonia siliqua L. y ahora es un acebuchal joven. El segundo es un acebuchal más maduro (“Bosque Maduro”, Fig. 1, punto 2) que ya estaba formado en el año 1956. Por último, se seleccionó una zona de acebuchal-encinar donde se está produciendo la sucesión hacia un encinar (“Bosque Mixto”, Fig. 1, punto 3), que ya estaba formado en el año 1956. En cada uno de los 3 bosques seleccionados se establecieron 6 parcelas de 100 m² (solo 3 en el caso del Bosque Mixto debido a la dificultad de acceso de la zona). Se trazaron polígonos de 12x12 m mediante el programa informático QGIS (QGIS, 2002). Las intersecciones de los polígonos dibujados serán las esquinas SO de las parcelas de muestreo. Una vez seleccionados los puntos que quedaban dentro de las zonas forestales, se seleccionaron 6 al azar (o 3 para el caso del Bosque Mixto). En cada punto se trazó un cuadrado de lado de 10 m. Se recopilaron los datos especificados a continuación de cada parcela entre los meses de julio y agosto de 2023.
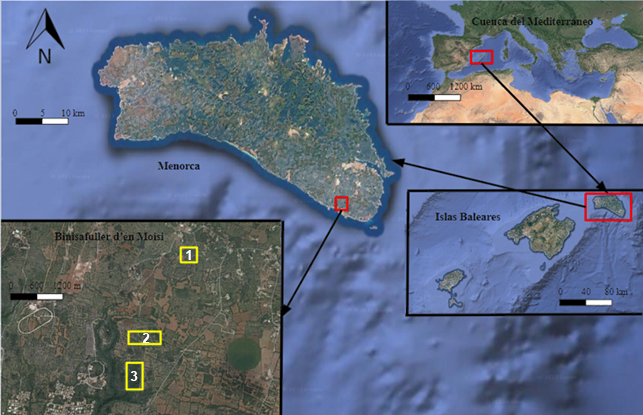
Figura 1. Localización del sitio de estudio en la Cuenca del Mediterráneo Occidental. Punto 1: “Antiguo Cultivo”, Punto 2: “Bosque Maduro”, Punto 3: “Bosque Mixto”.
Figure 1. Location of the study site in the Western Mediterranean Basin. Point 1: “Formerly Cultivated Land,” Point 2: “Mature Forest,” Point 3: “Mixed Forest.”
Caracterización dasométrica
Se consideraron individuos arbóreos aquellos cuyas yemas de crecimiento se encuentran a más de 2 m de altura, de acuerdo con la definición de macrofanerófitos (Smith, 1913; Serrada, 2008). Para cada individuo se anotaron: i) el nombre de la especie, ii) el diámetro a la altura del pecho (DBH), iii) el espaciamiento mínimo con el árbol más cercano, iv) la altura del árbol, y v) el ancho de la copa de N-S y de O-E. El DBH es una medida estándar del diámetro del tronco a 1.30 m, que se utilizará para calcular el área basal suponiendo que la sección del tronco es circular (Mostacedo y Fredericksen, 2000). El ancho de la copa se usará para calcular el área de copa de cada individuo suponiendo que la copa es elipsoidal y los anchos N-S y O-E corresponden a sus semiejes (Castillejo-González et al., 2010). Se calcularon las variables e índices dasométricos de interés para este estudio (Tabla 1) en cada parcela incluyendo: (i) las variables que dependen de cada árbol individualmente (Área Basal media, Altura media, Área de copa media, Coeficiente de Esbeltez medio y Grado de Imbrincación de Copas medio), (ii) los índices que resultan de relaciones aritméticas de las variables (Espaciamiento medio, Densidad arbórea y Área basimétrica, Índice de Hart-Becking, Fracción de Cabida Cubierta, Relación de Espaciamiento, Índice de Czarnowsky y Índice de Agregación de Clark y Evans), y (iii) el Índice de Valor de Importancia (IVI). El IVI pondera la importancia relativa de cada especie para un conjunto de muestras en función de la frecuencia relativa, la abundancia realtiva y la dominancia relativa representada por el área basal (Mostacedo y Fredericksen, 2000). Su valor se calcula para cada especie en cada uno de los tres bosques de estudio.
Tabla 1. Variables usadas en la caracterización dasométrica.
Table 1. Variables used in dasometric characterisation.
|
Índice |
Abreviación |
Fórmula |
Bibliografía |
|
Índice de Valor de Importancia |
IVI |
FR+AR+DR |
|
|
Área basal media (cm2) |
ABM |
μ(AB) |
|
|
Altura media (m) |
AM |
μ(AA) |
|
|
Área de copa media (m2) |
ACM |
μ(AC) |
|
|
Espaciamiento medio (m) |
EM |
μ(E) |
|
|
Densidad arbórea (árb. /ha) |
DE |
n/A*10000 |
|
|
Área basimétrica (m2/ha) |
AB |
∑AB/A*10000 |
|
|
Índice de Hart-Becking (%) |
IHB |
∑E/AD*100 |
|
|
Fracción de cabida cubierta (%) |
FCC |
∑AC/A*100 |
|
|
Relación de espaciamiento |
RE |
√[(μ(DC)2) /(μ(AB)²)] |
|
|
Coeficiente de esbeltez medio |
CEB |
∑AA/∑D*100 |
|
|
Grado de imbrincación de copas medio |
GIC |
∑DC/∑E |
|
|
Índice de Czarnowsky |
IC |
μ(AA)2*DE/10000 |
|
|
Índice de agregación de Clark y Evans |
ICE |
μ(E)*2*√(n/A) |
|
|
μ=media, FR=frecuencia relativa de la especie en el total de parcelas, AR=abundancia relativa de la especie en el total de parcelas, DR=dominancia relativa de la especie basada en el área basal en el total de parcelas, n=número de árboles, A=área en m², AB=área basal en m², E=espaciamiento medio en m, AD=altura dominante en m, AC=área de copa en m², AA=altura árbol en m, D=diámetro del tronco en m², DC=diámetro de copa en m. |
|||
Diversidad de especies de plantas
Para estudiar la diversidad de especies se realizaron inventarios de especies arbóreas y número de individuos en cada parcela, así como inventarios florísticos siguiendo la metodología de Braun-Blanquet (Braun-Blanquet y de Bolós, 1979; Campo y Duval, 2014). Se estudiaron tanto la diversidad local como la variación entre la composición de especies en función de la localidad de muestreo usando: curvas de acumulación de especies, cálculo del valor de equidad de las comunidades arbóreas, y una caracterización funcional. Para los análisis de diversidad se usó R software versión 4.4.1 (R Core Team, 2024). Las curvas de acumulación de especies se realizaron con los dos inventarios usando la función “specaccum” del paquete “vegan” (Oksanen et al., 2024). Para cuantificar la equidad en las comunidades arbóreas se usó la equidad de Simpson (Simpson, 1949), calculado con la función “diversity” también del paquete “vegan” (Oksanen et al., 2024). La caracterización funcional se hizo asignando a cada especie una forma vital siguiendo el criterio del Herbario Virtual del Mediterráneo Occidental (Herbari Virtual del Mediterrani Occidental, 2019).
Análisis estadísticos
Todos los cálculos estadísticos se realizaron usando R versión 4.5.2 (R Core Team, 2025). Se ha trabajado con dos tablas de datos: las variables e índices dasométricos, y los índices de diversidad. Para visualizar la relación de las variables en un espacio de pocas dimensiones se usó el Análisis de Componentes Principales (PCA, función rda del paquete vegan), ya que se trata de variables cuantitativas con las que puede trabajar con distancia euclidiana. Luego se realizaron Análisis de Varianzas (ANOVA, función Anova del paquete car; Fox y Weinsberg, 2019) para testar las diferencias entre zonas de muestreo para cada variable. La validación de los supuestos de la ANOVA basada en un modelo lineal se realizó mediante métodos gráficos usando: (i) gráficos de cuantiles normales de residuos para probar la normalidad, (ii) gráficos entre residuos y valores estimados para comprobar la homocedasticidad, y (iii) gráficos entre residuos y leverage para identificar puntos altamente influyentes. Si los residuos mostraron un patrón no normal se intentaron las transformaciones logarítmicas y radicales de los datos. Si los datos mostraron un patrón heterocedástico se planteó un modelo de cuadrados mínimos generalizados (GLS) con la función “gls” del paquete “nlme” (Pinheiro et al., 2023) considerando la variabilidad en función de cada zona de muestreo con la función “varIdent”. Si hay puntos altamente influyentes en el modelo, y no se corrige si efecto con las anteriores adaptaciones del modelo, se puede considerar usar un test no paramétrico, o prescindir de dicho punto altamente influyente. Los tests postHoc se realizaron calculando los intervalos de Tukey con la función “TukeyHSD”. Solo las variables o índices que tengan una significación estadística (p<0.05) entre el Antiguo Cultivo y las otras 2 zonas de muestreo serán consideradas válidas para interpretar su relación con la madurez del ecosistema. En caso de no validarse el modelo de regresión lineal, se procedió a una prueba de Kruskal-Wallis de la función “kruskal.test”. Los tests postHoc en este caso se realizaron con la prueba de Dunn y un ajuste de Bonferroni con la función “dunn.test” del paquete “dunn.test” (Dinno, 2024).
Resultados
Caracterización dasométrica
Los resultados obtenidos muestran diferencias significativas entre los bosques maduros (Bosque Maduro y Bosque Mixto) y el Antiguo Cultivo para la Área de Copa media, la Densidad media, el Coeficiente de Esbeltez y el Índice de Czarnowsky, tal y como se indica en la Tabla 2. Los resultados de las ANOVA coinciden bastante bien con el resultado del PCA (Fig. 2). De hecho, el primer eje del PCA sintetiza un gradiente claro de madurez forestal, separando los puntos del Antiguo Cultivo respecto las dos otras zonas de muestreo. Se aprecia un conjunto de variables que presentan valores más altos en el Antiguo Cultivo (destacando el Coeficiente de Esbeltez, la Densidad Arbórea y el índice de Czarnowsky), y otras que presentan valores más altos en las otras dos zonas de muestreo (Área Basal, Área de Copa media y Espaciamiento medio).
Los valores de IVI de O. europaea disminuyen desde el Antiguo Cultivo hasta el Bosque Mixto (Fig. 3). Al mismo tiempo, otras especies Phillyrea latifolia L. var. rodriguezii (P. Monts.) O. Bolòs & Vigo o Pistacia lentiscus L. van adquiriendo una importancia creciente. El último hecho por destacar es que O. europaea deja de ser la especie dominante en el Bosque Mixto donde predomina Q. ilex.
Tabla 2. Resultados de las variables dasométricas en cada localidad de muestreo con el p-valor obtenido.
Table 2. Results of the dasometric variables at each sampling location with the p-value obtained.
|
Índice |
Antiguo Cultivo |
Bosque maduro |
Bosque mixto |
Modelo |
r² |
p-valor (ANOVA) |
p-valor (Intervalos de Tukey o test de Dunn) |
|
ABM |
82.1 ± 36.9 |
169.5 ± 84.8 |
185.8 ± 83 |
Log-lineal |
0.465 |
0.0248* |
0.042 (1-2), 0.051 (1-3), 0.920 (2-3) |
|
AM |
3.7 ± 0.7 |
3.4 ± 0.5 |
3.4 ± 0.1 |
GLS |
0.097 |
0.508ns |
|
|
ACM |
2.9 ± 0.3 |
6.4 ± 3.8 |
4.9 ± 0.6 |
Lineal |
0.735 |
0.0007* |
0.001 (1-2), 0.004 (1-3), 0.999 (2-3) |
|
EM |
1.2 ± 0.2 |
2.2 ± 0.8 |
1.9 ± 0.4 |
Lineal |
0.476 |
0.0207* |
0.009 (1-2), 0.089 (1-3), 0.796 (2-3) |
|
DE |
1633 ± 250.3 |
583.3 ± 133 |
533.3 ± 57.7 |
Lineal |
0.909 |
5.513e-07* |
1e-6 (1-2), 6e-6(1-3), 0.9227 (2-3) |
|
AB |
13.8 ± 7.3 |
9.9 ± 4.9 |
9.7 ± 3.7 |
Lineal |
0.122 |
0.459ns |
|
|
IHB |
29.8 ± 8.6 |
59.4 ± 16.6 |
43.5 ± 5.1 |
Log-lineal |
0.617 |
0.00316* |
0.002 (1-2), 0.128 (1-3), 0.342 (2-3) |
|
FCC |
56.2 ± 23.6 |
36.1 ± 18.5 |
26.1 ± 3.7 |
Log-lineal |
0.387 |
0.053ns |
|
|
RE |
22.9 ± 1.9 |
21.6 ± 1.1 |
18.4 ± 3.6 |
GLS |
0.475 |
0.1288ns |
|
|
CEB |
46.5 ± 2.6 |
32.7 ± 5.3 |
27.4 ± 6.3 |
No lineal |
|
0.0072* |
0.018 (1-2), 0.009 (1-3), 0.739 (2-3) |
|
GIC |
2 ± 0.6 |
1.4 ± 0.6 |
1.3 ± 0.3 |
Lineal |
0.329 |
0.0916ns |
|
|
IC |
2.3 ± 1 |
0.7 ± 0.3 |
0.6 ± 0.1 |
Log-lineal |
0.764 |
0.00017* |
3.3e-4 (1-2), 0.001 (1-3), 0.965 (2-3) |
|
ICE |
1 ± 0.2 |
1.1 ± 0.3 |
0.9 ± 0.2 |
Lineal |
0.075 |
0.6259ns |
|
|
ABM = Área basal media, AM = Altura media, ACM = Área de copa media, EM = Espaciamiento medio, DE = Densidad arbórea, AB = Área basimétrica, IHB = Índice de Hart-Becking, FCC = Fracción de cabida cubierta, RE = Relación de espaciamiento, CEB = Coeficiente de esbeltez, ICV = Índice de copa viva, GIC = Grado de imbrincación de copas, IC = Índice de Czarnowsky, ICE = Índice de agregación de Clark y Evans, “ns” diferencias no significativas, “*” diferencias significativas con un nivel de significación de 0.05 y se indican las comparaciones por parejas como 1 = Antiguo cultivo; 2 = Bosque Maduro y 3 = Bosque Mixto. |
|||||||
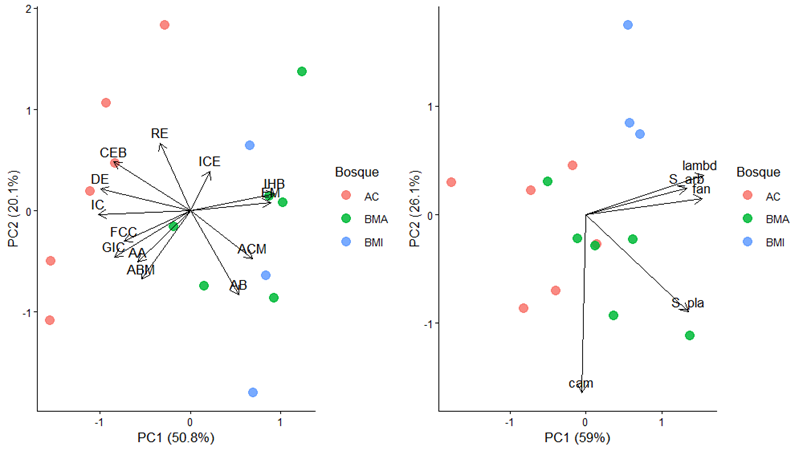
Figura 2. Ordenación de las variables dasométricas (izquierda) y las variables de diversidad (derecha).
Figure 2. Ordination of the dasometric (left) and diversity variables (right).
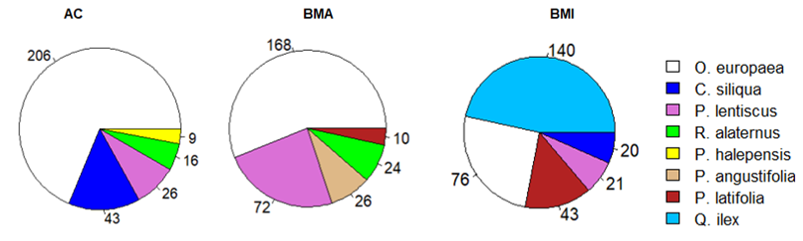
Figura 3. Representación del I.V.I. de cada especie arbórea en función de la localidad de muestreo.
Figure 3. Representation of the I.V.I. of each tree species as a function of sampling location.
Diversidad de especies de plantas
Los inventarios florísticos realizados en cada una de las parcelas se detallan en el Anexo. Los resultados obtenidos muestran diferencias en las curvas de acumulación de especies para los inventarios florísticos, pero no para los inventarios arbóreos (Fig. 4 A, B). El Bosque Maduro muestra más riqueza de plantas vasculares que el Antiguo Cultivo. Obsérvese que las curvas de acumulación de especies para el Bosque Mixto están claramente lejos de la saturación, por lo que seguramente se haya cometido un sesgo importante en la estimación de la riqueza de especies. Los análisis estadísticos con el índice de Simpson mostraron que existen diferencias significativas entre localidades de muestreo (Modelo lineal, r2= 0.639, F2,12=10.634, p=0.0022; Fig. 4 C). Las comparaciones por parejas muestran que los valores del Índice de Simpson del Antiguo Cultivo son mayores respecto a los dos bosques maduros (Intervalos de Tukey: p=0.013 para el Antiguo Cultivo y el Bosque Maduro y p=0.003 para el Antiguo Cultivo y el Bosque Mixto). El resultado de los análisis de varianzas para los inventarios florísticos mostró que: no existen diferencias significativas en la riqueza de especies (Model lineal, r2= 0.3716, F2,12=3.5485, p=0.0616), sí existen diferencias significativas en el número de fanerófitos (Model log-lineal, r2= 0.6294, F2,12=10.188, p=0.0026), y también existen diferencias significativas en el número de caméfitos (Model lineal, r2= 0.5724, F2,12=8.031, p=0.0061). Para otros grupos funcionales no se ha obtenido suficiente variabilidad para un análisis estadístico. Al realizar las curvas de acumulación de especies con los datos de número de caméfitos y de fanerófitos (Fig. 4 D, E) se aprecia que el Antiguo Cultivo presenta un número menor de fanerófitos, y el Bosque Mixto presenta un número menor de caméfitos (p<0.05 para los Intervalos de Tukey para cada caso). Estos patrones, probados estadísticamente, se observan también en el PCA, donde el grupo más distante es el Bosque Mixto (Fig. 2).
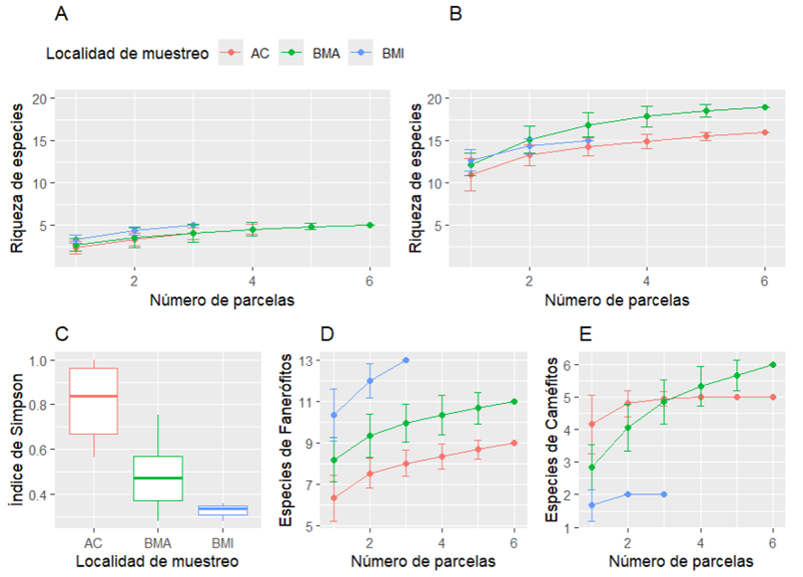
Figura 4. Curvas de acumulación de especies y valores del Índice de Simpson para las zonas de muestreo.
Figure 4. Species accumulation curves and Simpson's Index values for the sampling areas.
Discusión
Caracterización dasométrica
Hemos comprobado que diversos índices dasométricos varían significativamente entre bosques en un gradiente de madurez y sucesión forestal. Los índices dasométricos son un reflejo de las condiciones de crecimiento del arbolado por lo que es de esperar que no sean constantes en el tiempo (Mostacedo y Fredericksen, 2000). Los índices que miden la forma de los árboles individualmente muestran que los árboles de los bosques maduros son más gruesos y con mayores copas, a pesar de que tengan la misma altura. Consecuentemente, el Coeficiente de Esbeltez tiende a disminuir por su definición matemática (Serrada, 2008; Tabla 1). Luego, entendemos que los árboles tienen distinta forma, pero la causa de este patrón debe explicarse por las interacciones entre los individuos y su entorno.
Los índices que estudian la interacción entre individuos muestran que los bosques maduros presentan una menor Densidad Arbórea (DE), un mayor valor del Índice de Hart-Becking (IHB) y un menor valor del Índice de Czarnowsky (IC) (Tabla 2). Todos ellos son índices que cuantifican la espesura, es decir, el grado de interacción, relación o influencia que entre sí presentan los individuos del arbolado (Serrada, 2008). Los índices indican una disminución de la espesura con la maduración en todos casos, ya que la DE y el IC son directamente proporcionales a la espesura y IHB lo es inversamente. La disminución de la espesura ocurre por procesos de mortalidad llamados “aclareo natural”. El aumento de la competencia y de la presión ecológica de factores abióticos con el crecimiento de una masa forestal son los causantes (Zeide, 2001). Entonces, cuando crece un bosque joven, muchos individuos aparecen y al ir creciendo la competencia aumenta hasta tal punto que origina la muerte de los individuos que no consiguen desarrollarse. En este proceso se disminuye la espesura de la masa y también la competencia, hecho que permite a los individuos que quedan seguir creciendo y constituir un bosque más maduro.
Existe un gradiente en la importancia de O. europaea a través de los tres bosques estudiados (Fig. 3). Su importancia disminuye mientras que otras especies adquieren mayor peso en la comunidad, y en el Bosque Mixto ya deja de ser la especie más importante. Esto pone de manifiesto la gran capacidad de O. europaea como colonizadora y formadora de bosques de la que otras especies carecen. Quercus ilex, por ejemplo, solo crece bajo una formación arborescente preexistente, dado que solo germina y crece en condiciones de alta humedad (Fraga et al., 2014). Lo que también se concluye del análisis del IVI es que la comunidad se va volviendo más heterogénea cuando nuevas especies como Rhamnus alaternus L., Pistacia lentiscus L., Phillyrea latifolia L. var. rodriguezii (P. Monts.) O. Bolòs & Vigo y Phillyrea angustifolia L. van adquiriendo importancia. De hecho, lo mismo se observa en el análisis de diversidad donde se ve claramente que la equidad aumenta en comunidades más maduras. Otras especies como Pinus halepensis Miller y Ceratonia siliqua L. no tienen relevancia dado que el primero proviene en el Antiguo Cultivo de un pinar cercano y el segundo proviene en el Antiguo Cultivo y el Bosque Mixto de antiguos cultivos próximos. En el contexto de abandono agrícola generalizado en el Mediterráneo, estos resultados sugieren que los acebuchales pueden actuar como estadios facilitadores en la recuperación de bosques más complejos, con implicaciones directas para la planificación de la restauración ecológica y la conectividad forestal.
Diversidad de especies de plantas
Los métodos basados en la cuantificación del número de especies presentes no aportaron resultados significativos, en parte por disponer solo de tres parcelas en una de las zonas de muestreo (Fig. 4 A, B). Por otro lado, los resultados sí son más claros en los métodos que miden la estructura de las comunidades y no son dependientes del tamaño de las muestras. La riqueza específica por sí sola no tiene en cuenta la importancia de cada especie en una comunidad, con lo que al incorporar la distribución proporcional de cada especie se obtienen resultados más consistentes (Mostacedo y Fredericksen, 2000). El Índice de Simpson, que mantiene una correlación negativa con la equidad (Moreno, 2001), indica que la equidad es significativamente menor en el Antiguo Cultivo (Fig. 4 C). Esto tiene sentido si comparamos con los resultados del IVI que sugerían que la comunidad del Antiguo Cultivo es más homogénea que las otras. A su vez, este cambio en la equidad de las comunidades implica un cambio en la composición de estas.
Una manera de entender qué supone la sucesión de la comunidad de plantas vasculares es la diversidad funcional. En este caso se ha considerado la clasificación según la forma vital. La mayor abundancia relativa de especies de una forma de vida sobre otras refleja y está relacionada con las condiciones ambientales (Serrada, 2008). El número de fanerófitos parece ser un buen ejemplo de ello ya que aumenta significativamente en los bosques maduros (Fig. 4 D, E). El cambio en las condiciones ambientales como luz, humedad y competencia en la comunidad es el motor de este enriquecimiento de fanerófitos de las comunidades más maduras (Momo et al., 2016). Lejos de ser formaciones empobrecidas o transitorias sin valor ecológico, los acebuchales representan estadios funcionalmente relevantes que incrementan la heterogeneidad estructural del paisaje y amplían las oportunidades de establecimiento para especies arbóreas.
Conclusión
La madurez forestal y la sucesión ecológica estructuran tanto la arquitectura del arbolado como la composición de la comunidad vegetal en los acebuchales de Menorca. La maduración se traduce en cambios dasométricos predecibles (incremento del área basal y de la cobertura de copa, junto con una disminución de la espesura por aclareo natural) que reflejan una reorganización progresiva de las interacciones competitivas y permiten utilizar la estructura del arbolado como indicador funcional del estado de madurez del bosque. La sucesión de especies pone de manifiesto el papel facilitador de Olea europaea como especie pionera, que crea las condiciones para la incorporación progresiva de otras especies arbóreas y conduce a comunidades más heterogéneas y equitativas, con la eventual entrada de especies climácicas como Quercus ilex. Aunque la riqueza específica de la flora vascular se mantiene relativamente estable, se observan cambios de formas vitales a lo largo del gradiente de madurez, con un aumento de fanerófitos y una disminución relativa de caméfitos.
En conjunto, los acebuchales deben entenderse como sistemas dinámicos de transición dentro del mosaico agroforestal mediterráneo. La integración de indicadores dasométricos y de diversidad proporciona una base útil para evaluar su estado de madurez y su potencial sucesional, con implicaciones relevantes para la conservación y la restauración de bosques mediterráneos en un contexto de abandono agrícola y cambio global.
Contribución del autor
Marc Pons Sintes: Administración del proyecto, análisis formal, conceptualización, investigación, metodología, redacción.
Disponibilidad de datos y código
Los datos están disponibles en Figshare (Pons-Sintes, 2026; https://doi.org/10.6084/m9.figshare.31230829).
Financiación, permisos requeridos, potenciales conflictos de interés y agradecimientos
Esta investigación no ha recibido ninguna fuente de financiación y ha sido realizada solo con el propósito de ampliar la información de esta área de conocimiento.
Los autores/as declaran no tener ningún conflicto de intereses.
Agradezco al Sr. Carlos Maceda de Olives su predisposición a permitirme el muestreo en la finca de su propiedad Binisafúller de’n Moisi, y al Sr. Alejandro Guardia Camps por informarme sobre dicha finca que maneja. También al Dr. Miquel Capó Servera y al Sr. Pere Miquel Mir Rosselló por la revisión crítica del trabajo.
Referencias
Braun-Blanquet, J., de Bolòs, O., & Jo, J. L. (1979). Fitosociología: bases para el estudio de las comunidades vegetales (Vol. 820). Blume, Madrid, España.
Campo, A. M., & Duval, V. S. (2014). Diversidad y valor de importancia para la conservación de la vegetación natural: Parque Nacional Lihué Calel (Argentina). Anales de Geografía de la Universidad Complutense; 34(2), 25-42. http://dx.doi.org/10.5209/rev_AGUC.2014.v34.n2.47071
Castillejo-Gónzalez, I. L., Medina-Guerrero, J. M., García-Ferrer, A., Mesas-Carrascosa, F. J., & Sánchez-de la Orden, M. (2010). Satélite de altar resolución espacial en la determinación de la fracción de cabida cubierta en sistemas adehesados. In Congreso Nacional de Tecnologías de la Información Geográfica (14º. 2010. Sevilla) (62-71), Sevilla, Universidad de Sevilla. ISBN: 9788447212941.
Chang, C. C., & Turner, B. L. (2019). Ecological succession in a changing world. Journal of Ecology, 107(2), 503-509. https://doi.org/10.1111/1365-2745.13132
CIME. (5 de junio de 2022). Infraestructura de Dades Espacials de Menorca. Consell Insular de Menorca. https://ide.cime.es/visor/
Cutrina, J. C. (2003). El índice de Hart-Becking y su justa medida. Foresta, (24), 50-52. ISSN: 1575-2356.
Dinno, A. (2024). dunn.test: Dunn's Test of Multiple Comparisons Using Rank Sums. R package version 1.3.6, https://CRAN.R-project.org/package=dunn.test
Falek, W., Mascio, I., Gadaleta, S., Fanelli, V., Bechkri, S., Khelifi, D., … Montemurro, C. (2022). Morphological and eco-geographic variation in Algerian wild olives. Plants, 11(14), 1803. https://doi.org/10.3390/plants11141803
Fox, J., & Weisberg, S. (2019). An R Companion to Applied Regression, Third edition. Sage, Thousand Oaks CA. https://www.john-fox.ca/Companion/
Fraga, P., Truyol, M., Mascaró, C., Carreras, D., García, Ò., Pallicer, X., …. Seoane Barber, M. (2004). La vegetació del Migjorn de Menorca: un passeig descriptiu. En Història natural del Migjorn de Menorca: El medi físic i l'influx humà (pp. 53-72). Societat d'Història Natural de les Balears. ISBN: 84-609-3585-X.
Fraga, P., Estaún, I., Comas, M., & Cardona, E. (2014). Plantes de Menorca. Consell Insular de Menorca i Institut Menorquí d’Estudis, Maó, Menorca.
Gauquelin, T., Michon, G., Joffre, R., Duponnois, R., Genin, D., Fady, B., ... & Baldy, V. (2018). Mediterranean forests, land use and climate change: a social-ecological perspective. Regional Environmental Change, 18(3), 623-636. https://doi.org/10.1007/s10113-016-0994-3
Gianguzzi, L., & Bazan, G. 2019. The Olea europaea L. var. sylvestris (Mill.) Lehr. forests in the Mediterranean area. Plant Sociology, 56(2), 3-34. https://doi.org/10.7338/pls2019562/01
Gómez Sal, A. (2008). Componentes del valor del paisaje mediterráneo y el flujo de servicios de los ecosistemas. Ecosistemas, 16(3). Recuperado a partir de https://www.revistaecosistemas.net/index.php/ecosistemas/article/view/117
Herbari Virtual del Mediterrani Occidental. (2019) [usado 20 Sep 2023]. Disponible en: http://herbarivirtual.uib.es/.
Jansà, A. (2004). El clima del Migjorn. En Fornos, J. J., Obrador, A., Rosselló, V. M. (eds.), Història natural del Migjorn de Menorca: el medi físic i l’influx humà. Monografies de la Societat d’Història Natural de les Balears, núm. 11, 11, 39-52.
Kassout, J., Terral, J. F., Hodgson, J. G., & Ater, M. (2019). Trait-based plant ecology a flawed tool in climate studies? The leaf traits of wild olive that pattern with climate are not those routinely measured. PloS one, 14(7). https://doi.org/10.1371/journal.pone.0219908
LIFE RedBosques. (2018). Manual de campo para la identificación de rodales de referencia. Fase II: Identificación mediante parcelas. Ed. Fundación González Bernáldez, Madrid. Proyecto LIFE Redcapacita_2015. Deliverable B3.2. 53 pp.
Llorens, L., Gil, L., Tébar, F. J. 2007. La vegetació de l’illa de Mallorca. Bases per a la interpretació i gestió dels hàbitats. Associació Jardí Botànic de Sóller, Palma de Mallorca.
Médail, F., & Quezel, P. (1999). Biodiversity hotspots in the Mediterranean Basin: setting global conservation priorities. Conservation biology, 13(6), 1510-1513. https://www.jstor.org/stable/2641976
McIntosh, R. P. (1981). Succession and Ecological Theory. In: West, D.C., Shugart, H.H., Botkin, D.B. (eds), Forest Succession, Concepts and Application. Springer Advanced Texts in Life Sciences. Springer, New York, NY. https://doi.org/10.1007/978-1-4612-5950-3_3
Mercadal, B. (1962). Nota geológica y geográfica de San Luis. Revista de Menorca, 48, 51-63.
MITECO (2020). Cuarto Inventario Forestal Nacional, 2011-2018. Organismo Autónomo Parques Nacionales, Ministerio para la Transición Ecológica y el Reto Demográfico, Madrid, España. 89 pp. https://www.miteco.gob.es/es/biodiversidad/temas/inventarios-nacionales/inventario-forestal-nacional/cuarto_inventario.html
Ministerio de Agricultura (1971). Inventario Forestal Nacional Baleares. Ministerio de Agricultura, Dirección general de Montes, Caza y Pesca fluvial, Madrid, España. 86 pp.
Momo, S. M. C, Temgoua, L. F., Nogueguim, J. R., & Nkongmeneck, B. (2016). Comparison of plant communities between primary and secondary tropical forests of Mount Oku, Cameroon. Journal of Ecology and The Natural Environment, 8(10), 163-174. https://doi.org/10.5897/JENE2016.0598
Moreno, C. E. (2001). Métodos para medir la biodiversidad. M&T–Manuales y Tesis SEA, vol. 1. Zaragoza, 84 pp. ISBN: 84 – 922495 – 2 – 8.
Mostacedo, B., Fredericksen, T. (2000). Manual de métodos básicos de muestreo y análisis en ecología vegetal (Vol. 87). Santa Cruz, Bolivia: Proyecto de Manejo Froestal Sostenible (BOLFOR). http://www.bio-nica.info/biblioteca/mostacedo2000ecologiavegetal.pdf
Myers, N., Mittermeier, R. A., Mittermeier, C. G., Da Fonseca, G. A., & Kent, J. (2000). Biodiversity hotspots for conservation priorities. Nature, 403(6772), 853-858. ISSN: 1476-4687. https://doi.org/10.1038/35002501
Oksanen, J., Simpson, G., Blanchet, F., Kindt, R., Legendre, P., Minchin, P., …Weedon, J. (2024). vegan: Community Ecology Package. R package version 2.6-8. https://CRAN.R-project.org/package=vegan
Pausas, J. G., & Millán, M. M. (2019). Greening and browning in a climate change hotspot: the Mediterranean Basin. BioScience, 69(2), 143-151. https://doi.org/10.1093/biosci/biy157
Pinheiro, J., Bates, D., & R Core Team (2023). nlme: Linear and Nonlinear Mixed Effects Models. R package version 3.1-164. https://CRAN.R-project.org/package=nlme
Pons-Sintes, M. (2026). Dasometric data about sampling of wild olive tree forests. [Dataset]. Figshare. https://doi.org/10.6084/m9.figshare.31230829
QGIS Development Team. (2002). Free and Open-Source Geographic Information System, http://www.qgis.org/pt_PT/site/ [usado en 2023-06-23].
R Core Team (2024). R: A Language and Environment for Statistical Computing (Version 4.4.1) [Computer Software]. R Foundation for Statistical Computing. Vienna, Austria. https://www.R-project.org/.
R Core Team (2025). R: A Language and Environment for Statistical Computing (Version 4.5.2) [Computer Software]. R Foundation for Statistical Computing. Vienna, Austria. https://www.R-project.org/.
Rey, P. J., Alcántara, J. M. & Fernández, J. M., (2009). 9320 Bosques de Olea y Ceratonia. En: Hidalgo, R. (ed.), VV. AA., Bases ecológicas preliminares para la conservación de los tipos de hábitat de interés comunitario en España. Madrid: Ministerio de Medio Ambiente, y Medio Rural y Marino. Madrid, España. 66 p. https://jmferpal.webs.ull.es/Book_Chapters_files/9320%20Bosques%20de%20Olea%20y%20Ceratonia.pdf
Rita-Larrucea, J., & Payeras-Coll, T. (2006). Biodiversidad de las plantas vasculares de las Islas Baleares. Orsis: organismes i sistemes, 41-58. https://raco.cat/index.php/Orsis/article/view/53170
Rosselló, V. M., Fornós, J. J., & Gómez L. (2003). Introducció a la geografia física de Menorca. AGE - Universitat de València - Universitat de les Illes Balears - Societat d’Història Natural de les Balears.
Rubio-Camacho, E. A., González-Tagle, M. A., Himmelsbach, W., Ávila-Flores, D. Y., Alanís-Rodríguez, E., & Jiménez-Pérez, J. (2017). Patrones de distribución espacial del arbolado en un bosque mixto de pino-encino del noreste de México. Revista mexicana de biodiversidad, 88(1), 113-121. https://doi.org/10.1016/j.rmb.2017.01.015.
Serrada, R. (2008). Apuntes de selvicultura. Servicio de Publicaciones. EUIT Forestal. Madrid, España. 169-196. https://distritoforestal.es/images/Apuntes_de_Selvicultura_completo_2011.pdf
Smith, W. G. (1913). Raunkiaer's" life-forms" and statistical methods. Journal of Ecology, 1(1), 16-26. https://doi.org/10.2307/2255456
Simpson, E. H. (1949). Measurement of Diversity. Nature, 163, 688.
Vayreda, J., & Mezquida, J. A. A. (2020). Redbosques. Una red para la madurez forestal. Revista Montes, (139), 61-64. ISSN: 0027-0105.
Zeide, B. (2001). Natural thinning and environmental change: an ecological process model. Forest ecology and management, 154(1-2), 165-177. https://doi.org/10.1016/S0378-1127(00)00621-6
Anexo / Annex
Inventarios florísticos realizados en el trabajo / Floristic inventaries obtained during the field work.
|
Especie / Parcela |
C.1 |
C.2 |
C.3 |
C.4 |
C.5 |
C.6 |
M.1 |
M.2 |
M.3 |
M.4 |
M.5 |
M.6 |
B.1 |
B.2 |
B.3 |
Forma vital |
|
Olea europaea L. |
4 |
4 |
4 |
4 |
4 |
3 |
4 |
4 |
3 |
3 |
3 |
2 |
2 |
1 |
1 |
Fanerófito |
|
Asparagus acutifolius L. |
1 |
+ |
+ |
+ |
r |
0 |
+ |
r |
+ |
+ |
1 |
+ |
1 |
0 |
+ |
Caméfito |
|
Ceratonia siliqua L. |
2 |
0 |
2 |
1 |
2 |
1 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
Fanerófito |
|
Pistacia lentiscus L. |
3 |
3 |
3 |
3 |
3 |
3 |
2 |
3 |
4 |
4 |
4 |
4 |
3 |
2 |
2 |
Fanerófito |
|
Rhamnus alaternus L. |
2 |
1 |
2 |
1 |
+ |
+ |
r |
1 |
+ |
+ |
1 |
1 |
1 |
1 |
1 |
Fanerófito |
|
Phagnalon saxatile (L.) Cass. |
r |
0 |
r |
+ |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
Caméfito |
|
Asparagus albus L. |
+ |
+ |
+ |
+ |
+ |
r |
+ |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
Caméfito |
|
Asparagus horridus L. in J.A. Murray |
1 |
+ |
r |
r |
0 |
r |
r |
1 |
0 |
0 |
r |
0 |
0 |
0 |
0 |
Caméfito |
|
Solanum nigrum L. subsp. nigrum |
r |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
Terófito |
|
Rubia peregrina L. |
+ |
+ |
+ |
+ |
+ |
0 |
1 |
1 |
+ |
+ |
+ |
1 |
+ |
+ |
+ |
Fanerófito |
|
Clematis cirrhosa L. |
+ |
+ |
+ |
+ |
0 |
0 |
r |
+ |
+ |
+ |
+ |
+ |
+ |
0 |
0 |
Fanerófito |
|
Centaurium pulchellum (Swartz) Druce |
+ |
r |
r |
+ |
r |
+ |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
Caméfito |
|
Piptatherum miliaceum (L.) Coss. subsp. miliaceum |
+ |
0 |
0 |
0 |
r |
0 |
r |
r |
+ |
+ |
+ |
0 |
0 |
0 |
0 |
Hemicriptófito |
|
Smilax aspera L. |
0 |
0 |
1 |
+ |
+ |
+ |
2 |
2 |
1 |
2 |
2 |
1 |
1 |
+ |
+ |
Fanerófito |
|
Lonicera implexa Ait. |
0 |
0 |
0 |
1 |
0 |
0 |
+ |
0 |
r |
+ |
0 |
2 |
1 |
0 |
0 |
Fanerófito |
|
Rubus ulmifolius Schott |
0 |
0 |
0 |
0 |
+ |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
Fanerófito |
|
Ruscus aculeatus L. |
0 |
0 |
0 |
0 |
0 |
0 |
1 |
+ |
r |
0 |
0 |
0 |
0 |
r |
+ |
Fanerófito |
|
Vinca difformis Pourr. |
0 |
0 |
0 |
0 |
0 |
0 |
1 |
1 |
0 |
0 |
r |
0 |
0 |
0 |
0 |
Caméfito |
|
Phillyrea angustifolia L. |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
2 |
+ |
0 |
2 |
3 |
1 |
1 |
Fanerófito |
|
Brachypodium retusum (Pers.) Beauv. |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
+ |
+ |
0 |
+ |
1 |
+ |
+ |
Caméfito |
|
Calicotome spinosa (L.) Link |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
r |
0 |
0 |
1 |
2 |
0 |
1 |
Fanerófito |
|
Phillyrea latifolia L. var. rodriguezii (P. Monts.) O. Bolòs & Vigo |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
+ |
0 |
1 |
1 |
2 |
1 |
Fanerófito |
|
Teucrium capitatum L. |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
r |
0 |
0 |
0 |
Caméfito |
|
Juniperus phoenicea L. subsp. turbinata (Guss.) Nyman |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
r |
0 |
0 |
0 |
Fanerófito |
|
Quercus ilex L. |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
2 |
3 |
3 |
Fanerófito |
|
Cistus monspeliensis L. |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
1 |
1 |
2 |
Fanerófito |
|
La letra corresponde a la localidad de muestreo (C = Antiguo Cultivo, M = Bosque Maduro, B = Bosque Mixto) y el número al número de parcela. |
||||||||||||||||